ООО "ПРОПИОНИКС"
| пн-пт с 09:00 до 18:00 | |
Часть II. «Курса лекций по общей микробиологии и основам вирусологии»
КУРС ЛЕКЦИИ ПО ОБЩЕИ МИКРОБИОЛОГИИ И ОСНОВАМ ВИРУСОЛОГИИ
В двух частях (часть 2)

ОГЛАВЛЕНИЕ
Введение
Важность микроорганизмов для поддержания биосферы долгое время недооценивали, считая, что при таких малых размерах они не могут оказывать важного влияния на экологические системы. По современным представлениям, существенную часть живой биомассы на Земле составляет биомасса прокариот и им принадлежит активная роль в превращениях органических и неорганических соединений в окружающей среде.
Клетки прокариот метаболитически более активны, чем клетки эукариот, и этим обусловлена их важная экологическая роль. Жизнедеятельность микроорганизмов в окружающей среде проявляется заметнее в их активности, чем в видимом присутствии.
Во 2-й части «Курса лекций по общей микробиологии и основам вирусологии» рассмотрены закономерности жизнедеятельности микроорганизмов в природных условиях, которые существенно отличаются от условий в лаборатории.
В естественных местообитаниях микроорганизмы почти всегда находятся в условиях дефицита субстратов, а не их избытка. Кроме того, в природных условиях микроорганизмы растут в присутствии субстратов разных типов, в которых редко присутствует только один вид микроорганизмов; чаще всего каждый микроорганизм конкурирует с другими видами или образует с ними кооперацию.
Условия в естественных местообитаниях, как правило, нестабильны; они изменяются во времени, следуя суточным и годичным циклам.
Самым главным воздействием, которое прокариоты оказывают на окружающую среду, является их способность обеспечивать круговорот основных химических элементов, необходимых для построения биологических систем.
Глава 7
ЭКОЛОГИЧЕСКИЕ НИШИ ПРОКАРИОТ
В изучении экологии микроорганизмов используют два подхода: 1) аутоэкологический и 2) синэкологический.
Аутоэкологический подход позволяет изучать в лабораторных условиях штаммы, выделенные в чистой культуре, в отношении их метаболитической активности, используемых ими субстратов, реакции на изменение условий (влажность, освещённость, температура, рН среды и др.), метаболитической адаптации к изменяющимся условиям окружающей среды. Эти исследования позволяют выяснить способы существования микроорганизмов в природных условиях и влияние окружающей среды на них, но при этом невозможно выяснить, как влияет жизнедеятельность микроорганизмов на окружающую среду.
Синэкологический подход применяют в тех случаях, когда необходимо определить характер формирования сообщества микроорганизмов и зависимости его членов друг от друга в природной экосистеме. В природных условиях на микроорганизмы одновременно влияют комплексы разнообразных и взаимодействующих между собой факторов, включая высшие организмы (растения, животные, люди), поэтому синэкологическое исследование значительно сложнее, чем аутоэкологическое.
§ 7.1. Доступность основных источников питания и энергии в экосистемах
Свет – основной источник энергии почти во всех экосистемах. Видимый свет, достигающий поверхности Земли, состоит в основном из инфракрасного и незначительной части ультрафиолетового излучения.
Микроорганизмы обладают различными механизмами защиты от повреждающего действия ультрафиолета; например, они синтезируют поглощающие его пигменты (каратиноиды или меланины). Фотосинтезирующие организмы содержат светособирающие пигмент-белковые комплексы (антенны) для улавливания солнечного света, используемого при фотосинтезе.
Водоросли и водные микроорганизмы не нуждаются в сильной защите от светового излучения, поскольку сама вода действует как защитный барьер. Светопроницаемость воды зависит от длины волны падающего света. Инфракрасный свет в значительной степени поглощается молекулами воды. Интенсивность ультрафиолетового света меньше снижается за счёт поглощения, но с глубиной падает из-за рассеяния и обратного рассеяния. На изменение качества света с глубиной влияют его поглощение растворёнными соединениями (например, фульвокислотами), которые поглощают прежде всего синий свет, рассеиваемый суспендированными в воде частицами, а также поглощение света в определённых областях спектра водорослями и другими фотосинтезирующими организмами в зависимости от содержания в них пигментов.
Интенсивность и качественный состав света в толще воды в значительной степени варьируют в различных местообитаниях и зависят от качества воды, а также от количества и типов присутствующих в ней фотосинтезирующих организмов.
Органическое вещество (источник углерода) синтезируется в природе в основном фотосинтезирующими растениями, в первую очередь высшими, а также водорослями и цианобактериями. Живые растения являются пищей для животных, а отмершие растения, трупы и экскременты животных и выделения растений служат питательными веществами для гетеротрофных микроорганизмов, главным образом бактерий и грибов, которые окисляют их до СО2, воды и неорганических солей, используемых затем фотосинтезирующими организмами.
Самые распространённые субстраты, подвергающиеся микробному разложению, – это биополимеры. Растения состоят примерно на 50 % из целлюлозы; кроме того, в их состав входят лигнин (10 – 25 %), гемицеллюлоза и пектин (10 – 20 %), белки (5 – 10 %), липиды (2 – 5 %) и нуклеиновые кислоты (до 2 %). Животные ткани богаты белками (50 – 80 %), липидами (10 – 15 %), полисахаридами (5 – 10 %), а нуклеиновых кислот содержат не более 5 %.
Мономерные субстраты легко разлагаются многими микроорганизмами, в то время как полимерные разлагают только специализированные микроорганизмы.
Микробное разложение органического вещества не всегда заканчивается полной минерализацией. В присутствии кислорода специфические или неспецифические оксигеназы превращают ароматические и алифатические субстраты в фенольные или спиртовые соединения, которые затем образуют радикалы и полимеризуются с образованием крупных агрегатов.
В почве с этим связано превращение древесины в гумус; в полимерные вещества, составляющие гумус, могут дополнительно включаться такие компоненты, как аминокислоты, сахара и разнообразные олигомеры, вследствие чего скорость разложения гумуса существенно снижается. Почвенный гумус обычно содержит кроме ароматических производных лигнина значительную долю алифатических соединений, производных сахаров и белков. Молекулярная масса гумусовых веществ может возрастать до нескольких дальтон. В воде озер присутствует эквивалент этого почвенного вещества – водные гуминовые кислоты, молекулярная масса которых составляет от 1,5 до 150 кДа. Их состав зависит от поступления извне лигнинсодержащих остатков. Гумусовые вещества медленно преобразуются под действием микробов, химических и фотохимических факторов, поэтому химические свойства их компонентов постепенно меняются.
Полимерные субстраты могут присутствовать в природной среде в изобилии, например, в поверхностном слое лесной почвы до 70 % сухого вещества, и их разложение происходит медленно. Деградации растительных полимеров значительно способствуют жуки, земляные черви, улитки, ногохвостки, термиты, жвачные животные, которые механически уменьшают размер частиц субстратов и облегчают микробам использование субстратов как внутри своего пищеварительного тракта, так и в экскрементах. Простейшие захватывают мелкие частицы посредством фагоцитоза, в то время как прокариоты вначале частично разлагают полимеры вне клеток с помощью экзоферментов и поглощают только низкомолекулярные субстраты.
Концентрация свободных мономерных органических соединений в природной среде, как правило, низка, в результате того что они быстро и эффективно поглощаются разнообразными организмами, входящими в микробное сообщество.
Концентрация свободных сахаров варьирует от нескольких микромолей в относительно богатых средах обитания, например в ризосфере (почва непосредственно у корней растений), до пикомолей в океанской воде.
Свободные аминокислоты в водной среде и в почве обычно присутствуют в наномолярной концентрации.
Низкая концентрация мономерных органических веществ в стабильных природных местообитаниях отражает уровень разлагающей микробной активности и наличие у микроорганизмов разнообразных транспортных систем с высоким сродством к субстратам.
Кислород необходим для жизнедеятельности облигатно аэробных микроорганизмов, но для анаэробных он токсичен.
Молекулярный кислород присутствует в атмосферном воздухе в количестве до 21 % (или 9 ммоль/л). Аэробные микроорганизмы выдерживают такую концентрацию этого потенциально токсичного газа и используют его для получения энергии в процессе дыхания. В водных средах при 4 – 20 °С равновесная концентрация кислорода составляет 300 – 400 мкМ. При растворении атмосферных газов происходит относительное обогащение воды кислородом по сравнению, например, с N2 и Ar, вследствие его более высокой полярности, но небольшой запас кислорода, растворённого в воде, может весьма быстро потребляться микробами. Концентрация органических субстратов, близкая к 10 мг/л (расчёт как для эквивалентов сахаров), достаточна для полного потребления микроорганизмами растворённого в воде кислорода при 15 °С. То есть процессы микробного разложения в водной среде, требующие участия кислорода, зависят от интенсивного восполнения его запаса в растворённом виде посредством, в частности, вихревой конвекции. Растворимость кислорода снижается с увеличением солёности воды. Морская вода с концентрацией соли 3,5 (масса/объем) содержит при одной и той же температуре на 20 % меньше кислорода, чем пресная. В присутствии света кислород может вызывать повреждающие эффекты, так как воздействие ультрафиолета на компоненты клеток способствует образованию кислородных радикалов, разрушающих нуклеиновые кислоты.
Азот составляет примерно 16 % сухого вещества биомассы и является вторым по количеству элементом после углерода в составе клеток. Неорганический азот доступен в природе живым организмам как источник энергии и питания в форме нитрата, нитрита, аммиака и молекулярного азота. Концентрация общего связанного неорганического азота в различных природных экосистемах варьирует в пределах 1 – 500 мкМ. В составе клеток азот обычно присутствует в восстановленной форме; он поглощается, а также высвобождается при разложении микробных клеток в виде аммиака. В природных средах, богатых О2, связанный азот присутствует преимущественно в виде нитрата, для ассимиляции которого требуется предварительное восстановление до аммиака в процессе ассимиляционной нитроредукции. Способность к ассмимиляции молекулярного азота, довольно широко распространенная среди прокариот, связана с активностью сложного по структуре фермента нитрогеназы. Процесс азотфиксации требует большого количества энергии в форме АТФ и строго регулируется во избежание её потерь. Везде, где восстанавливается нитрат или окисляется аммиак, присутствует также нитрит, концентрация которого in situ обычно не превышает микромолярного уровня; в более высокой концентрации нитрит оказывает повреждающее действие вследствие своего мутагенного действия.
Неорганические соединения серы. Сера содержится в клетках в количестве примерно 0,2 % сухого вещества биомассы и представляет собой необходимый питательный элемент. В живых клетках сера присутствует обычно в восстановленной форме и ассимилируется в виде сероводорода (H2S). Это соединение серы стабильно только в строго анаэробной среде. В присутствии кислорода H2S реагирует химически с кислородом с образованием тиосульфата (S2O2-), сульфита (HSO–) или молекулярной серы (S0), и на этом основан лабораторный метод удаления с помощью сероводорода минимальных количеств кислорода при культивировании строгих анаэробов. Спонтанное окисление H2S/HS- сравнительно быстро протекает при рН 7,5 – 8,5 и медленно при более низких значениях рН; другой максимум скорости этой реакции имеет место при рН 11. В присутствии каталитических количеств тяжёлых металлов или окисляющих серу микроорганизмов сульфит может также полностью окисляться до сульфата – формы, в которой сера обычно встречается в средах, богатых кислородом. Для ассимиляции сульфата клетки должны обладать сульфатредуктазной системой. В пресных водах, содержащих кислород, сульфат присутствует в концентрациях 50 – 300 мкМ. Исключение составляют воды, богатые гипсом (CaSO4); в насыщенной гипсом воде при 25 °С концентрация сульфата близка к 14 мкМ. Морская вода очень богата сульфатом – концентрация SO42- составляет в ней 28 мкМ. Выделяющийся в донных осадках H2S реагирует с ионами тяжёлых металлов, в первую очередь железа:
Fe2+ + H2S →FeS + 2H+
Поскольку оксиды и карбонаты железа, а также других тяжёлых металлов обычно присутствуют в водоёмах в избытке, концентрация свободных H2S и HS- в осадках, даже морских, обычно ниже 100 мкМ. Судьфид Fe(II) (FeS) осаждается в форме микрокристаллов, которые поглощают свет всего видимого спектра. Вследствие этого отложения судьфида железа окрашены в чёрный цвет и бескислородные осадки часто имеют окраску от тёмно-серой до чёрной.
FeS может далее взаимодействовать с H2S, образуя пирит (FeS2), в котором сера имеет степень окисления –1:
FeS + H2S → FeS2 + H2
В этой реакции высвобождается некоторое количество свободной энергии (∆G0` = –38,4 кДж/моль), однако к настоящему времени нет сведений о том, что её осуществляют микроорганизмы. Образующийся пирит стабилен в отсутствие сильных окислителей и может быть основным соединением серы в глубоких пресноводных или морских осадках.
Молекулярная сера (S0) почти нерастворима в воде; в одном литре чистой воды при 25 °С её растворяется не более 5 мг (0,16 мкМ). В природных средах она присутствует вследствие этого не в воде, а главным образом в осадках как незначительная фракция общей серы, меньшая, чем фракция пирита и сульфита, либо внутри клеток метаболизирующих серу бактерий (глобулы серы). Более значительные отложения серы накапливаются вокруг горячих сероводородных источников, где H2S взаимодействует с кислородом воздуха с образованием молекулярной серы.
Фосфор присутствует в природных средах в форме фосфата, т. е. имеет степень окисления +5. Он не восстанавливается в реакциях биологического преобразования энергии. Известно несколько фосфорорганических соединений, в которых присутствуют связи С—Р или С—Р—С. Фосфорные минералы обычно слаборастворимы, как в случае апатитов [Ca5(F,OH,Cl)(PO4)3] или фосфата железа (III) (FePO4). Концентрация свободного фосфора в природных водах поэтому низкая: от 10-7 до 10-6 М. Фосфат является существенным компонентом биомассы, присутствуя в ней в количестве примерно 0,5 % сухого вещества клеток. Среднее соотношение элементов в биомассе водорослей, соотношение Редфилда, в озёрах составляет 106C : 16N : 1P. Из-за низкой растворимости фосфата его уровень обычно лимитирует первичную продукцию, и незначительно возросшее поступление фосфора может резко повысить общую продуктивность. То есть фосфат служит важнейшим фактором, от которого зависит продуктивность водорослей в экосистемах пресноводных озер. По имеющимся данным, гетеротрофные бактерии успешно конкурируют с водорослями и цианобактериями за растворённый неорганический фосфат в озёрах.
Железо – один из наиболее важных компонентов земной коры, но в живых клетках его содержание не превышает 0,01 %, при контакте железа с водой образуются его гидроксиды и оксиды, или оксигидраты. Особое биологическое значение имеют взаимопревращения Fe(II) и Fe(III), лежащие в основе активности, например, цитохромов и Fe-S-белков. В бескислородной среде Fe+2 растворим в воде до концентрации 10-7 – 10-6 М в зависимости от концентрации карбоната и, таким образом, присутствует в достаточном для микробных клеток количестве. При избытке H2S происходит осаждение FeS и концентрация свободного Fe+2 падает до 10-9 М и менее. В присутствии кислорода при нейтральном значении рН происходит осаждение Fe+3 в форме Fe(OH)3 и FeO(OH) и концентрация свободного Fe3+ в чистой кислородсодержащей воде составляет примерно 10 – 18 М. Свободный Fe+3 недоступен для микробных клеток в этих условиях, в связи с этим аэробные бактерии обладают специальными системами поглощения ионов железа с участием хелатирующих соединений – сидефоров. В качестве хелатирующих агентов выступают в природных средах также гуминовые кислоты и фульвокислоты, в результате концентрация растворённого трёхвалентного железа поддерживается на низком уровне.
Окислительно-восстановительный потенциал перехода Fe(II) → Fe(III) зависит от значения рН. При рН меньше 2,4 он соответствует стандартному окислительно-восстановительному потенциалу +770 мВ, так как обе формы, Fe2+ и Fe3+, хорошо растворимы и присутствуют в равных концентрациях. При повышении рН трёхвалентное железо осаждается в формах Fe(OH)3 и FeO(OH) и доминирует свободный Fe2+, в результате этого эффективный окислительно-восстановительный потенциал сдвигается до значения примерно +100 мВ при нейтральном значении рН. То есть энергетика восстановления и окисления железа значительно варьирует в зависимости от рН.
Аналогично в присутствии марганца, степень окисления которого изменяется от Mn(II) до Mn(IV), растворимость в воде этих двух ионных форм значительно различается и зависит от рН. Существуют также относительные стабильные смешанные оксиды (Mn3O4), в форме которых марганец труднодоступен для микроорганизмов. Реальные величины окислительно-восстановительного потенциала зависят от активности протонов при рН больше 6,0, и, как правило, они являются примерно на 500 мВ более высокими (электроположительными), чем редокс-потенциал железа.
§ 7.2. Участие микроорганизмов в окислительно-восстановительных превращениях субстратов
Окислительно-восстановительные реакции различных типов, катализируемые микроорганизмами, составляют определённую иерархию по степени предпочтительности. Всегда наблюдается последовательность окислительно-восстановительных реакций, характерная для всех изученных микробных экосистем, – в толще пресной воды, в морских осадках, увлажнённой почве, морском заливе, активном иле или микробном мате в горячем источнике (рис. 1).

Рис. 1. Последовательность окислительно-восстановительных реакций в процессе минерализации органического вещества
В аэробных условиях акцептором электронов водорода при окислении органического вещества в микробных популяциях является молекулярный кислород. Микроорганизмы используют О2 как конечный (терминальный) акцептор электронов в дыхательной цепи, а так-же как косубстрат в оксигеназных реакциях, необходимых для активации инертных субстратов. Кислород слабо растворим в воде и медленно диффундирует через её толщу, поэтому он быстро расходуется. В отсутствие кислорода бактерии используют в качестве конечного акцептора электронов нитрат, который при этом восстанавливается через нитрит до газообразного азота, N2O или аммиака. В отличие от кислорода нитрат или его восстановленные производные могут служить только акцепторами электронов, но не косубстратами в реакциях активации инертных субстратов. Многие аэробные бактерии восстанавливают нитрат до молекулярного азота, легко переключаясь с аэробного дыхания на нитратное и обратно. В присутствии кислорода нитратредукция не всегда полностью подавляется, что давно было известно для некоторых подробно изученных лабораторных штаммов бактерий. Как установлено в недавних исследованиях, ряд штаммов Pseudomonas, Aeromonas, Moraxella и Arthrobacter способен восстанавливать нитрат при насыщении среды воздухом до 80 %, т. е. осуществлять восстановление нитрата в аэробных условиях.
Некоторые бактерии-бродильщики восстанавливают нитрат только до нитрита; этим в значительной мере объясняется накопление нитрита в желудочно-кишечном тракте при «нитратной нагрузке», например при употреблении загрязнённой нитратом воды.
Важность процесса нитратредукции с образованием аммиака долгое время недооценивали. Некоторые анаэробные бактерии, в том числе сульфатредукторы, образуют аммиак из нитрата и таким путём сбрасывают больше электронов в расчёте на молекулу нитрата, чем при денитрификации. Следовательно, аммонификацию нитрата следует рассматривать как предпочтительный процесс в средах, богатых органическим веществом, но бедных нитратом.
Полное окисление органических субстратов (даже полимеров) возможно при использовании молекулярного кислорода и нитрата. После исчерпания нитрата в процессе разложения органических веществ совместно участвуют различные группы микроорганизмов.
Бактерии-бродильщики превращают полимерные или мономерные соединения в классические продукты брожения, в том числе органические кислоты, такие как молочная и янтарная, спирты, газообразный водород и диоксид углерода. Продукты первичного брожения окисляются далее бактериями с использованием железа (III) и марганца (IV) в качестве акцепторов электронов.
К бактериям, способным восстанавливать железо, относятся представители видов Geobacter metallireducens и Shewanella spp., способные окислять разнообразные органические вещества (сахара, аминокислоты, ароматические соединения). Как предполагают некоторые исследователи, перенос электронов на оксид железа, вероятно, связан с запасанием энергии.
Восстановление марганца не имеет существенного значения в пресных водоёмах, но может иметь большое значение в местах, где накапливается марганец, например в некоторых морских осадках, в Балтийском море или в некоторых скальных породах. Какую роль этот процесс играет в жизнедеятельности бактерий (получают ли они метаболитическую энергию при восстановлении марганца), в настоящее время неизвестно.
Сульфатредуцирующие бактерии в присутствии сульфатов полностью окисляют продукты первичного брожения до диоксида углерода с параллельным восстановлением сульфата до сульфида. Но эти бактерии не могут самостоятельно воздействовать на сложные полимерные субстраты, поэтому они существуют в тесной кооперации с бактериями-бродильщиками, осуществляющими первичное брожение. То есть сульфатзависимое окисление сложных органических соединений – это двухступенчатый процесс, в котором метаболическую энергию получают оба партнёра.
Сера играет незначительную роль в качестве альтернативного акцептора электронов в озёрных осадках, её восстанавливают специализированные бактерии, а также бродильщики и сульфатредуцирующие бактерии. После восстановления серы и сульфата до сульфида начинается процесс метаногенеза как последний этап анаэробного разложения, который осуществляют метаногенные архебактерии.
Там, где сульфат содержится в незначительной концентрации, например в пресных водах, метаногенез становится доминирующим конечным процессом превращения органических субстратов (одноуглеродных соединений и ацетата). Метаногенные архебактерии могут использовать очень ограниченное число субстратов – только одноуглеродные соединения и ацетат.
Большое разнообразие продуктов брожения, образующихся при использовании метаногенными архебактериями немногих субстратов, обеспечивается участвующими в процессах вторичного брожения синтрофными бродильщиками или облигатными протонорепродукторами. Эти бактерии обитают в тесной кооперации с метаногенными архебактериями и превращают жирные кислоты, спирты, пропионат и бутират в ацетат, водород и одноуглеродные соединения, используемые метаногенами.
Таким образом, микроорганизмы в природе выполняют функцию катализаторов, ускоряющих химические реакции. Они могут конкурировать с традиционными химическими реакциями, такими как кислородзависимое окисление сульфида или двухвалентного железа при нейтральном значении рН или восстановление нитроароматических соединений, при которых микробные коферменты действуют как катализаторы либо продукты их метаболизма (Fe2-) выполняют роль субстратов. Не всегда в сложных природных системах можно провести различие между микробной активностью и чистыми химическими процессами, но есть несколько основных признаков, по которым можно отличить микробную активность от химически катализируемых процессов:
- микроорганизмы катализируют процессы, которые без их участия происходили бы очень медленно или протекали бы иным образом, например окисление сульфида до сульфата вместо сульфита, тиосульфата и др;
- микроорганизмы высокоспецифичны в отношении субстрата и сдвигают реакцию в определённом направлении;
- для реакций, протекающих с участием микроорганизмов, характерно наличие оптимальных значений в узких границах температуры (около 40 °С), рН (около 4 единиц), содержания кислорода, осмотической силы, окислительно-восстановительного потенциала и др.;
- в процессе микробной реакции может увеличиваться её скорость из-за размножения микробных клеток и увеличения количества катализатора;
- активность микроорганизмов в процессе реакции зависит от присутствия косубстратов (источников C, N, S , Р и др.);
- реакции с участием микроорганизмов чувствительны к некоторым токсичным веществам (тяжёлым металлам, фенолам и др.);
- микроорганизмы образуют внеклеточные полимеры, которые входят в состав структуры их местообитания, что влияет на такие процессы, как диффузия, ограничение переноса.
§ 7.3. Кинетика микробного роста в природных экосистемах
Закономерности роста и размножения микроорганизмов рассмотрены в первой части курса лекций (гл. 3, § 3.4, 3.5). В данном параграфе уделено внимание особенностям роста в природных экосистемах в условиях круговорота веществ.
В природе микроорганизмы обычно находятся в условиях недостатка питательных веществ или голодания, при которых наиболее важной является способность к выживанию, нежели быстрый рост популяции при избытке питательных веществ. Влияние условий голодания на микроорганизмы в лабораторных условиях изучают на штаммах энтеробактерий Escherichia coli, Klebsiella, кокках Paracoccus и других, для которых эти условия существования являются обычными.
Разделяют несколько типов голодания при изучении выживания микроорганизмов в зависимости от источника энергии и питания. Например, голодание по источнику углерода, который является источником как питания, так и энергии, является более тяжелой ситуацией, чем голодание по источникам серы, фосфора или азота, которые являются только источниками питания, и их недостаток препятствует только росту, не влияя на процессы поддержания жизнедеятельности.
Для выживания в условиях голодания бактерии используют следующие адаптации: первая сводится к увеличению поглощения субстрата при любой его концентрации, а вторая – к снижению потребностей клеток в энергии. В природных микробных популяциях существуют оба типа адаптаций и даже возможно их сочетание.
Увеличение поглощения субстрата осуществляется из-за возрастания числа транспортных систем (пермеаз и др.) или за счёт увеличения поверхности клетки посредством образования простек (стебельков) у таких бактерий, как Caulobacter, Prosthecochloris и Stella, которые обитают в условиях низкого содержания питательных веществ.
Образование спор также является одним из способов выживания бактерий в условиях голодания, потому что обеспечивает независимость от питания и защиту от высыхания и нагревания. У других групп микроорганизмов встречаются другие формы, предназначенные для выживания, такие как цисты, микроспоры, акинеты.
Большинство грамотрицательных бактерий не образуют спор при неблагоприятных условиях, но уменьшают размер клеток из-за снижения потребности в энергии и питательных веществах. Это явление (карликовые формы) часто можно наблюдать у бактерий в морской воде и чистых (бедных органическими соединениями) водоёмах. Наиболее хорошо феномен карликовости изучен у бактерий рода Vibrio.
Образование слизи также часто встречается у голодающих бактерий, которое помогает им поддерживать протонный градиент, мембранный потенциал, сохранять воду при высыхании и способствовать прикреплению к субстратам. В условиях окружающей среды микробные клетки почти всегда прикреплены к поверхностям или образуют агрегаты, внутри которых либо содержатся минеральные частицы, либо их нет. Образование биоплёнок характерно для микроорганизмов, способных прикрепляться к поверхностям. Примером могут служить технические сооружения, водопроводные и канализационные трубы, трубы для водных растворов на предприятиях пищевой и бумажной промышленности в тех случаях, когда они не подвергаются стерилизации. Иногда эти биоплёнки могут превращаться в слизистые слои, различные по толщине и неоднородные по консистенции. При изучении микроструктуры биоплёнок было установлено, что они не всегда представляют собой сплошной слой, в их структуре могут быть каналы и открытые участки, через которые в биоплёнку могут поступать растворённые вещества и даже мелкие частицы.
Таким образом, микробные сообщества характеризуются специфической динамикой роста и разложения субстратов, которые отражают все типы взаимодействий, известных для структурированных экосистем, ограниченных (лимитированных) по кислороду.
§ 7.4. Кооперативные взаимодействия с участием микроорганизмов
Кооперация между различными видами микроорганизмов распространена не так широко, как конкуренция. Совместное существование двух различных организмов называется симбиозом (от греч. simbiosis – совместная жизнь). Различают несколько вариантов полезных взаимоотношений: метабиоз, мутуализм, комменсализм, сателлизм.
Метабиоз – это взаимоотношение между микроорганизмами, при котором один микроорганизм использует для своей жизнедеятельности продукты жизнедеятельности другого организма. Метабиоз характерен для почвенных нитрифицирующих бактерий, использующих для метаболизма аммиак – продукт жизнедеятельности аммонифицирующих почвенных бактерий.
Под мутуализмом понимают такие взаимовыгодные взаимоотношения между разными организмами, при которых один вид питается за счет своего хозяина, но не только не причиняет ему никакого вреда, а, напротив, приносит пользу, например, синтезирует для него витамины или другие необходимые вещества. Примером такой кооперации являются лишайники – симбиоз гриба и сине-зеленой водоросли. От клеток водоросли гриб получает органические вещества, в свою очередь поставляя водоросли минеральные соли и защищая от высыхания.
Комменсализм (от лат. commensalis – сотрапезник) – это форма сосуществования особей разных видов, при котором выгоду из симбиоза извлекает один вид, не причиняя другому вреда. Комменсалами являются бактерии – представители нормальной микрофлоры человека. Но при известных условиях комменсалы, которыми обычно являются условно-патогенные бактерии (стафилококки, стрептококки, грамотрицательные бактерии), могут стать виновниками различных, чаще всего гнойно-воспалительных заболеваний.
Сателлизм – это явление усиления роста одного вида микроорганизма под влиянием другого. Например, колонии дрожжей или сарцин, выделяя в питательную среду метаболиты (витамины, аминокислоты и др.), стимулируют рост вокруг них колоний микроорганизмов других видов, неспособных синтезировать эти вещества.
Помимо кооперации микроорганизмы могут находится друг с другом в антогонистических взаимоотношениях, которые выражаются в виде неблагоприятного воздействия одного вида микроорганизма на другой, приводящего к повреждению и даже к гибели последнего. Микроорганизмы–антагонисты распространены в почве, воде и организме человека и животных. Примером таких взаимоотношений является взаимодействие представителей нормальной микрофлоры толстого кишечника человека (бифидобактерий, лактобацилл, кишечной палочки и др.) и гнилостной микрофлоры (бациллы, клостридии, псевдомонады и др.). Одной из форм антогонистических отношений является паразитизм.
Паразитизм – это существование микроорганизмов за счет хозяина, сопровождающееся нанесением ему серьезного ущерба в виде того или иного заболевания.
Механизм антагонистических взаимоотношений разнообразен: образование антибиотиков (продуктов метаболизма микроорганизмов, подавляющих развитие микроорганизмов других видов), большая скорость размножения, продукция бактериоцинов (колицинов), продукция органических кислот и других продуктов, изменяющих рН среды.
§ 7.5. Ассоциации с различными системами организма животных
Поверхность тела и слизистые оболочки животных в зависимости от наличия на них легкоразлагаемых субстратов, как и всех живых организмов, заселены различными микроорганизмами (бактериями, мицелиальными грибами, дрожжами и простейшими). Наиболее предпочтительным местообитанием для микроорганизмов является пищеварительный тракт, потому что в нем в избытке присутствуют питательные вещества, частично переваренные ферментами хозяина, и имеются оптимальные условия для жизнедеятельности: большое количество воды; стабильные значения рН и температуры.
Численность бактерий в кишечнике взрослого человека более чем в 10 раз превышает число клеток его собственного организма.
Роль микроорганизмов в пищеварении зависит от типа питания животного (плотоядное, растительноядное или травоядное, всеядное, детритофаги). Схема общего строения пищеварительного тракта позвоночных представлена на рис. 2.

Рис. 2. Строение пищеварительной системы позвоночных (по Й. Ленгелеру, Г. Древсу, Г. Шлегелю, Б. Шинку, 2005)
Пища поступает в ротовую полость, где механически измельчается и подвергается воздействию амилаз (ферментов слюны). Затем она поступает через пищевод в желудок, где среда сильнокислая, и оттуда – в тонкий кишечник, в котором происходит всасывание низкомолекулярных веществ. Пищевой комок (химус), сформировавшийся в результате прохождения через тонкий кишечник, поступает в толстый кишечник, где обезвоживается, и здесь же оставшиеся субстраты метаболизируются кишечными бактериями. В толстом кишечнике формируются фекалии, которые выходят через заднепроходное отверстие. Эта схема пищеварения характерна для плотоядных животных, потому что мясная пища не нуждается в дополнительной обработке и относительно легко переваривается.
Микроорганизмы, обитающие в пищеварительном тракте позвоночных, и животное-хозяин являются конкурентами в борьбе за поступающую пищу. Большая часть микробов, поступающая в пищеварительный тракт с пищей, погибает под воздействием соляной кислоты в желудке. Простейшие и бактерии-бродильщики, пройдя все отделы пищеварительного тракта, закрепляются только в толстом кишечнике и используют для своего питания те питательные вещества, которые не всосались в тонком кишечнике (табл. 1).
Таблица 1 Некоторые виды прокариот в микрофлоре пищеварительного тракта растительноядных животных
|
№ п/п
|
Группа микроорганизмов
|
Функция
|
|
1
|
Ruminococcus albus
|
Разложение целлюлозы
|
|
2
|
Butyrivibrio fibrisolvens
|
|
|
3
|
Fibrobacter succinogenes
|
|
|
4
|
Clostridium locheadii
|
|
|
5
|
Fibrobacter succinogenes
|
Разложение гемицеллюлозы
|
|
6
|
Butyrivibrio fibrisolvens
|
|
|
7
|
Ruminococcus albus
|
|
|
8
|
Lachnospira multiparus
|
|
|
9
|
Selenomonas ruminantium
|
Разложение крахмала и сахара
|
|
10
|
Succinimonas amylolytica
|
|
|
11
|
Bacteroides ruminicola
|
|
|
12
|
Streptococcus bovis
|
|
|
13
|
Selenomonas lactilytica
|
Разложение лактата
|
|
14
|
Megasphaera elsdenii
|
|
|
15
|
Veillonella spp.
|
|
|
16
|
Selenomonas ruminantium
|
Разложение сукцината
|
|
17
|
Veilonella parvula
|
|
|
18
|
Methanobrevibacter ruminantium
|
Метаногенные археи
|
|
19
|
Methanomicrobium mobile
|
Растительноядные животные в большей степени, чем плотоядные, зависят от участия микроорганизмов в процессе пищеварения. Жизнедеятельность этих микроорганизмов обеспечивается тем, что у растительноядных животных пищеварительный тракт состоит из ряда отделов для сбраживания, которые расположены как перед желудком (рубец или до желудочная пищеварительная камера), между тонким и толстым кишечником (в слепой кишке), так и в толстом кишечнике (послежелудочная пищеварительная камера). В рубце (дожелудочной пищеварительной камере) микроорганизмы разлагают поступившую пищу и подготавливают её для поступления в желудок и тонкий кишечник. В желудке и тонком кишечнике часть исходной пищи и микробная биомасса подвергаются дальнейшему перевариванию, а микроорганизмы разлагают те остатки пищи, которые животное не может использовать, и делают их доступными для всасывания в толстом кишечнике. Такой тип питания является одновременно примером и конкуренции, и кооперации микроорганизмов и организма животного-хозяина.
§ 7.6. Нормальная микрофлора тела человека
С первых минут жизни ребёнок, развивавшийся в стерильных условиях и родившийся стерильным, вступает в контакт с микрофлорой окружающей среды. Микроорганизмы, находящиеся в воздухе, на предметах ухода, населяющие организм матери и сотрудников родильного дома, в течение короткого времени заселяют кожные покровы ребёнка и слизистые оболочки, сообщающиеся с внешней средой. В результате этого формируется новая экологическая система: организм человека и населяющая его микрофлора. Эта система очень динамична, так как взаимоотношения в ней – это симбиоз микроорганизмов с макроорганизмом, который может проявляться в форме мутуализма, комменсализма или паразитизма.
Нормальная микрофлора тела – это микрофлора здорового организма человека. Она неодинаково представлена в количественном и качественном отношении на различных участках тела. Причина этого – неодинаковые условия обитания на коже и слизистых оболочках разных органов. Заселение тела человека микроорганизмами происходит в результате оседания пыли и проникновения их вместе с вдыхаемым воздухом, принимаемой пищей и т. д. Общее количество микроорганизмов, обнаруживаемых у взрослого человека, достигает 1014, что почти на порядок больше числа клеток всех тканей человека. В разных участках человеческого тела в соответствии с условиями обитания формируются ассоциации (биотопы) микроорганизмов, состоящие из разнообразных видовых сочетаний. На слизистых оболочках, особенно желудочно-кишечного тракта, представители нормальной микрофлоры обитают в виде двух форм: часть из них располагается в просвете, другая часть заключена в высокогидратированный матрикс, который состоит из экзополисахаридномуциновых компонентов, образуя своеобразную биопленку. Заключенные в эту биопленку микроорганизмы обладают по сравнению с просветными более высокой устойчивостью к действию физических, химических и биологических факторов. В случае когда эти факторы подавляют компенсаторные возможности экологической системы (хозяин и его микрофлора), могут возникать микроэкологические нарушения, результатом которых могут быть различные патологические состояния и другие неблагоприятные последствия (формирование антибиотикоустойчивых и атипичных штаммов, образование новых микробных биотопов и т. п.).
Микрофлора кожи. Кожные покровы обильно заселены микроорганизмами, особенно в местах, защищенных от действия света и высыхания (подмышечные впадины, межпальцевые и паховые складки, промежность). Количество бактерий на 1 см2 варьирует от нескольких единиц до сотен тысяч особей. По расчетам П. Ремленже, общее число микробов на коже одного человека колеблется от 100 млн до 1 млрд. Существенное значение имеет гигиеническое содержание кожных покровов. Наиболее постоянен состав микрофлоры не на ее поверхности, где он нередко имеет случайный характер, а в глубоких слоях ее, в области устьев сально-волосяных фолликулов. Наиболее частыми представителями кожной микрофлоры являются Staphylococcus epidermidis, S.saprophyticus и грибы рода Candida, реже встречаются дифтероиды, микрококки. На кожных покровах условия для размножения бактерий не очень благоприятны, так как на них губительно действуют высыхание, десквамация эпителия, образующиеся перекиси, кислая рН и другие антимикробные факторы. При нормальном состоянии кожных покровов человек не ощущает присутствия на них микроорганизмов, но при травмах, потертостях, потливости, экзематозных поражениях они тотчас же дают о себе знать, вызывая процессы гнилостного разложения, отторжения эпидермиса, воспаление сальных и потовых желез и нагноительные процессы. Сдвиг микрофлоры кожи в сторону увеличения грамотрицательных бактерий служит указанием на нарушение ее нормального состава.
Микрофлора верхних дыхательных путей представлена стрептококками, дифтероидами, моракселлами, псевдомонадами. Основная масса микрофлоры рото- и носоглотки приходится на долю зеленящего стрептококка (до 99 % всех микроорганизмов). Постоянно, но в меньшем количестве встречаются нейссерии, коринебактерии (дифтероиды) и стафилококки. На состав микрофлоры оказывают влияние бактерицидные вещества слюны (лизоцим, ингибин), фагоцитарная активность лейкоцитов, адсорбционные свойства слизи и ресничек эпителиальных клеток. При спокойном дыхании человек с каждым вдохом поглощает от 1500 до 14 000 и более микробных клеток, но все они задерживаются в верхних отделах дыхательных путей (это было доказано исследованиями плеврального воздуха при естественном пневмотораксе). Слизистая оболочка гортани, трахеи, бронхов и альвеолы здорового человека не содержат микроорганизмов.
Микрофлора мочеполового тракта менее обильна, но по видовому составу разнообразна и представлена стафилококками, дифтероидами, стрептококками, микобактериями, бактероидами, фузобактериями. В наружных отделах половых органов и мочевыводящих путей чаще всего обнаруживаются микобактерии смегмы и фузобактерии. Во влагалище здоровых женщин преобладают молочнокислые палочки Додерлейна и дифтероиды, значительно реже встречаются стрептококки, стафилококки, пептострептококки, клостридии и грамотрицательные палочки. Число бактерий мочеполового тракта значительно уменьшается по мере удаления от его наружных отделов. Полость матки, фаллопиевы трубы и мочевой пузырь здоровых людей обычно микробов не содержат. На состав микрофлоры мочеполового тракта оказывают влияние бактерицидные свойства секретов половых путей, а у женщин – высокая кислотность влагалищного секрета (рН 4,0 – 4,6), которая регулируется молочнокислой палочкой Додерлейна (разные виды рода Lactobacillus) за счет образуемой ею молочной кислоты при расщеплении углеводного компонента слизи, прежде всего гликогена. Кислая среда угнетает рост стафилококков и грамотрицательных бактерий (рис. 3).

Рис. 3. Молочнокислые бактерии, возможно, палочки Додерлейна в ассоциации с вагинальным эпителием
Микрофлора желудочно-кишечного тракта. Микрофлора полости рта представлена многочисленными видами аэробных и анаэробных микроорганизмов, так как для них здесь имеются вполне благоприятные условия – щелочная реакция слюны, наличие пищевых остатков, благоприятная для размножения температура (37 °С). Сразу после рождения ребенка в его ротовой полости формируется аэробная флора – кокки, палочки; с прорезыванием зубов появляются анаэробные бактерии, в том числе вибрионы, спириллы, спирохеты, клостридии. В полости рта происходит непрерывное загрязнение микробами и самоочищение под влиянием лизоцима, ингибина и других факторов, вследствие чего формируется более или менее постоянная микрофлора, наиболее частыми представителями которой являются стафилококки, стрептококки, грибы Candida, лактобактерии, нейссерии, спирохеты, вибрионы, постоянно присутствуют анаэробы – вейллонеллы, бактероиды, пептострептококки. Иногда из слюны здоровых людей выделяют простейших, аспергиллы, дрожжи и другие микроорганизмы.
Пищевод у здоровых людей обычно свободен от микроорганизмов или заселен ими очень мало.
Желудок. В связи с кислой реакцией среды, неблагоприятной для развития микроорганизмов, в желудке сформировалась специфическая микрофлора: дрожжи, сарцины, грибы, лактобактерии, стафилококки, стрептококки, кампилобактерии и другие, но не гнилостные бактерии (всего до 30 видов) Изменение состава микрофлоры, в частности появление гнилостных бактерий, – признак нарушения нормальной функции желудочной секреции.
Тонкий кишечник. Микрофлора необильная и довольно однообразная: лактобактерии, энтерококки, бифидумбактерии, E.coli и некоторые другие. Размножению бактерий препятствуют бактериостатическое действие желчи, секретов слизистой оболочки и секреторные иммуноглобулины класса IgA. В ряде случаев, например, всвязи с нарушением желудочной секреции, или с повреждением слизистой оболочки кишечника в результате радиационного облучения, или вследствие заболевания печени, желчных путей и поджелудочной железы, или иммунодефицита, у людей развивается синдром избыточной колонизации тонкого кишечника. Он заключается в том, что в тонкой кишке резко увеличивается концентрация бактериальной флоры, аналогичной по видовому и количественному составу микрофлоре толстого кишечника. Такое накопление в тонком кишечнике необычной для него микрофлоры может привести к различным нарушениям его функции.
Микрофлора толстого кишечника наиболее обильна и многообразна. Особенности условий обитания для микроорганизмов в толстом кишечнике состоят в том, что это орган не секреторный, а экскреторный, в нем отсутствует лизоцим, лимфоидная ткань представлена менее мощно, в то же время здесь благоприятные рН, температура, обилие питательных веществ и т. п. Формирование микрофлоры толстого кишечника начинается с первым вздохом ребенка, но в первые три дня, пока ребенок питается молозивом (молоко, обогащенное иммуноглобулинами матери), в толстом кишечнике размножаются разнообразные, в том числе гнилостные бактерии. Как только он начинает питаться грудным молоком матери, гнилостные бактерии исчезают и формируется постоянная микрофлора, в которой преобладают бактерии, образующие при ферментации глюкозы молочную кислоту. В толстом кишечнике обнаружено более 260 видов бактерий, общая биомасса их составляет около 1,5 кг (табл. 2).
Таблица 2 Доминирующие виды микроорганизмов, выделенные из содержимого толстой кишки человека [21]
|
№
п/п
|
Вид микроорганизма
|
Численность на грамм сухого вещества
|
|
1
|
Bacteroides thetaiotaomicron
|
1011
|
|
2
|
Bacteroides vulgatus
|
1011
|
|
3
|
Bacteroides fragltis
|
1010
|
|
4
|
Bacteroides distasonis
|
1011
|
|
5
|
Bacteroides ovatus
|
1010
|
|
6
|
Streptococcus intestinalis
|
1010
|
|
7
|
Bifidobacterium adolescentis
|
1010
|
|
8
|
Peptococcus prevotii
|
1010
|
|
9
|
Peptostreptococcus productus
|
1010
|
|
10
|
Штамм J 52 (гомоацетогенный)
|
1011
|
|
11
|
Штамм CS7H (гомоацетогенный)
|
109
|
Микрофлору толстого кишечника можно разделить на следующие 4 группы:
- Основную массу микрофлоры составляют строгие анаэробы, не образующие спор: грамположительные бактерии рода Bifidobaclerium и грамотрицательные бактерии семейства Bacteroidaceae. На долю бифидобактерий и бактероидов приходятся до 96 – 99 % всей микрофлоры толстого кишечника. Они выделяются из испражнений даже при разведении 10-10 – 10-12 степени.
- Вторую группу составляют факультативные анаэробы, представленные главным образом грамотрицательной E.coli и грамположительными энтерококками и молочнокислыми палочками рода Lactobacillus (спор не образуют). На их долю приходятся 1 – 4 % всей микрофлоры.
- Третью группу составляет так называемая остаточная микрофлора, на которую приходятся 0,01 – 0,001 % всех микроорганизмов толстого кишечника. К этой группе принадлежат Staphylococcus, Pro teus, Candida, Clostridium, Pseudomonas.
- К четвертой группе относятся различные другие представители семейства Enterobacteriaceae, которые могут временно или постоянно обнаруживаться в кишечнике и вызывать кишечные инфекции (Salmonella, Shigella, Enterobacter и другие роды).
Роль нормальной микрофлоры в организме хозяина (человека и животных) была изучена на примере животных, которые испытывают недостаток в любой бактериальной флоре (далее «животные без микробов») по сравнению с обычными животными, которые имеют типичную нормальную флору. В этих экспериментах было показано следующее.
- Нормальная микрофлора синтезирует и секретирует витамины сверх их собственных потребностей. Например, кишечные бактерии продуцируют витамины К и В 12, молочнокислые бактерии производят некоторые витамины группы Б. Животные без микробов могут ощущать дефицит витамина К до такой степени, что необходимо им включать его в рацион питания.
- Нормальная микрофлора предотвращает колонизацию патогенных бактерий, конкурируя с ними посредством прикрепления к тканям или за основные питательные вещества. Полагают, что наиболее важно это действие в ротовой полости, кишечнике, на коже и эпителии влагалища. В некоторых экспериментах животных без микробов можно было заразить 10 клетками сальмонелл, в то время как для заражения обычных животных требуется инфекционная доза около 106 клеток.
- Нормальная микрофлора может противодействовать другим бактериям через образование веществ, которые подавляют рост или убивают те разновидности бактерий, которые не свойственны нормальной микрофлоре. Кишечные бактерии производят широкий спектр самых разнообразных веществ от неспецифичных жирных кислот и пероксидов до высокоспецифичных бактериоцинов, которые угнетают или убивают другие бактерии.
- Нормальная микрофлора стимулирует развитие некоторых тканей, а именно слепой кишки и некоторых лимфатических тканей (Пейеровых бляшек) в желудочно-кишечном тракте. Слепая кишка у животных без микробов увеличена, имеет тонкие стенки и заполнена жидкостью по сравнению с этим органом у нормальных животных. Также у животных без микробов плохо развиты лимфотические ткани кишечника по сравнению с таковыми у обычных животных.
- Микроорганизмы нормальной микрофлоры стимулируют образование перекрёстно-реагирующих (кроссреактивных) антител.
Клетки бактерий нормальной микрофлоры являются антигенами по отношению к организму животных и вызывают образование иммунного ответа, в частности, антителомедиаторного иммунного ответа. Известно, что низкие уровни антител против компонентов нормальной микрофлоры перекрёстно реагируют с некоторыми родственными патогенными бактериями и тем самым предотвращают инфекции и инвазии. Антитела, образованные против антигенных компонентов нормальной микрофлоры, иногда рассматривают как «естественные» антитела, и такие антитела отсутствуют у животных без микробов.
Таким образом, кожные покровы и слизистые оболочки макроорганизмов заселены различными видами микроорганизмов, которые образуют с макроорганизмом единую целостную экологическую систему. Состав и состояние микрофлоры зависят от макроорганизма, но, в свою очередь, и микрофлора, особенно толстого кишечника, оказывает существенное и многообразное влияние на макроорганизм.
Воздействие микрофлоры на макроорганизм проявляется в следующем:
- Она является одним из важных факторов естественной резистентности организма, так как проявляет высокоантагонистическое действие по отношению к другим бактериям, в том числе патогенным, препятствуя их размножению в организме. На это обстоятельство давно указывал И. И. Мечников: «Природа пользуется конкуренцией безобидных микробов, чтобы помешать поселению патогенных микробов». Ему принадлежит идея употребления в пищу молочно-кислых продуктов с целью подавления развития в кишечнике гнилостных бактерий и продления жизни человека.
- Микрофлора своими антигенными факторами стимулирует развитие лимфоидной ткани организма и таким образом также способствует развитию неспецифической и опосредованной специфической резистентности.
- Микрофлора, особенно толстого кишечника, участвует в процессах пищеварения, в том числе в обмене холестерина и желчных кислот.
- Важная роль микрофлоры заключается также в том, что она обеспечивает организм человека различными витаминами, которые синтезируются ее представителями (витамины В1, В2, В6, B12, К, никотиновая, пантотеновая, фолиевая кислоты и др.). Эти витамины обеспечивают большую часть потребностей в них организма.
Однако представители нормальной микрофлоры не всегда приносят только пользу. При определенных условиях, в частности при воздействии факторов, снижающих естественную резистентность, особенно в результате ионизирующего облучения, практически все представители нормальной микрофлоры, за исключением бифидобактерий, могут стать виновниками различных эндогенных инфекций, чаще всего гнойно-воспалительных заболеваний с различной локализацией: ангины, менингиты, циститы, отиты, сепсисы, нефриты, аппендициты, абсцессы, флегмоны и т. п. Нередко после перенесенных кишечных заболеваний и особенно после длительного и нерационального применения антибиотиков возникают дисбактериозы.
Дисбактериоз – изменение количественного соотношения и состава нормальной микрофлоры организма, главным образом его кишечника, при котором происходят уменьшение количества или исчезновение обычно составляющих её микроорганизмов и появление в большом количестве редко встречающихся или несвойственных ей микробов.
Обычно это соотношение нарушается в сторону увеличения количества факультативно-анаэробной или остаточной микрофлоры, главным образом грамотрицательных палочек, стафилококков, дрожжеподобных грибов Candida или Clostridlum. Дисбактериозы развиваются потому, что антибиотики, особенно с широким антимикробным спектром, действуют не только на возбудителя заболевания, но и на чувствительных к ним представителей нормальной микрофлоры, угнетая их размножение. В этих условиях те микроорганизмы, на которые антибиотики не действуют, начинают беспрепятственно размножаться, особенно если понижена и естественная резистентность организма. Чаще всего устойчивыми являются стафилококки, грибы Candida и различные грамотрицательные палочки (кишечная палочка, протей, псевдомонады). Это и приводит к развитию дисбактериозов. Наиболее тяжелыми формами дисбактериозов, представляющими уже самостоятельные заболевания, являются стафилококковые пневмонии, стафилококковые сепсисы, кандидомикозы (в том числе генерализованные) и антибиотико-ассоциированные колиты, особенно стафилококковый и псевдомембранозный колит, вызываемый Clostridium dijficile. Для лечения дисбактериозов кишечника и колитов рекомендуется применение специальных бактерийных препаратов, способствующих восстановлению нормальной микрофлоры: колибактерин (высушенная взвесь живых бактерий E.coli штамм M-17, антагонистически активного в отношении шигелл Флекснера и Зонне), бифидумбактерин (высушенная взвесь живых бифидобактерий), лактобактерин (высушенная взвесь антагонистически активных штаммов лактобактерий), бификол (высушенная взвесь живых антагонистически активных бифидобактерий и E.coli M-17), бактисубтил или других, сходных по назначению и составу биопрепаратов.
§ 7.7. Ассоциации микроорганизмов с растениями
Микроорганизмы локализуются в побегах, цветках и корнях растений, их ассоциации с растениями так же, как и с животными, могут быть как благоприятными, так и неблагоприятными для хозяина. Если микроорганизмы вызывают увядание и гибель растений, то их считают патогенными, и такие микроорганизмы изучает раздел частной микробиологии – фитопатология. Наиболее фитопатогенными и часто выделяемыми от больных растений являются представители царства Fungi и бактерии родов Erwinia, Pseudomonas, Xanthomonas, Agrobacterium и др.
Микрофлора (микроорганизмы, обитающие на поверхности растений) подразделяется на временно (транзиторная) и постоянно присутствующую (конститутивную). Наибольшее количество микроорганизмов обнаруживают на нижней стороне листьев, там, где находятся устьица, потому что вокруг них повышенная влажность и на поверхность выделяются растворённые сахара. В этих условиях обитают бактерии-бродильщики, относящиеся к родам Lactobacillus, Leuconostoc, а также представители родов Propionibacterium, Xanthomonas и Pseudomonas. Эти бактерии препятствуют развитию в области устьиц фитопатогенных бактерий, потому что образуют кислоту аналогично бактериям, обитающим на поверхности кожи животных и человека. Состав и количество микроорганизмов на поверхности листьев изменяется в зависимости от времени года. Так, весной преобладают бактерии, в то время как осенью – грибы, поскольку увеличивается влажность. В чашечках цветков растений обычно содержится нектар, который является селективной средой для некоторых видов микроорганизмов, в частности для дрожжей Cаndida reukaufii.
Ризосфера. Этот термин был введён в 1904 г. Л. Хильтнером. Ризосфера – это узкая зона почвы вокруг корня растения в диапазоне примерно нескольких миллиметров, в которой она находится в тесном контакте с поверхностью корней. В зависимости от почвенных условий и типа растений толщина ризосферного слоя варьирует от нескольких миллиметров до нескольких сантиметров. Корни растений выделяют в ризосферу растворённые органические вещества, такие как сахара, гликолат, ацетат, сукцинат, малат и другие, которые служат источником питания для микроорганизмов, обитающих в ризосфере. Микробные сообщества ризосферы обычно специфичны для вида растений. Поскольку растения выделяют до 20 % органического углерода в прикорневую зону и сдвигают соотношение азот/углерод до условий относительной азотной недостаточности, в ризосфере обитают преимущественно азотфиксирующие бактерии и поставляют связанный азот в данную экосистему. Бактерии ризосферы способствуют поддержанию благоприятных условий для питания растений, тем что выделяют хелатообразующие соединения (сидерофоры), способные мобилизовать (связывать) тяжёлые металлы (железо), и переводят их в доступную для использования растениями форму. Лектины, выделяемые корнями растений, способны распознавать микробные клетки как те, которые поддерживают рост растений, так и фитопатогенные, и способствуют прикреплению только клеток благоприятных видов. Примером кооперации азотфиксирующих бактерий с высшими растениями являются бактерии рода Azospirillum и однодольные растения (райграс, каллы или белокрыльник), которые не образуют совместных структур, и бактерии, не прикрепляясь к корням, используют органические вещества, выделяемые растением, и обогащают ризосферу азотом; а бактерии Acetobacter diazotrophicus обитают в межклеточных пространствах стеблей сахарного тростника.
Микориза – это тоже один из типов кооперации между микроорганизмами и растениями, это ассоциация корней деревьев и травянистых растений с грибами. Многие грибы классов аскомицеты и базидиомицеты образуют ассоциации с корнями хвойных (сосна, ель, лиственница и др.) и широколиственных (дуб, береза и др.) деревьев. Мицелий грибов прорастает в корневые волоски и образует структуру, которая более эффективно поглощает минеральные вещества и воду, чем мицелий гриба и корень дерева по отдельности.
Бактерии-бродильщики, железобактерии, сульфатредукторы и метаногены создают условия для роста растений на гидроморфных почвах при выращивании риса или тростника. Представители семейства Enterobacteriaceae из родов Klebsiella и Enterobacter способствуют высокой продуктивности этих экосистем, потому что обладают азотфиксирующей активностью и могут обитать в тесной ассоциации с таким болотным растением, как осока Carex elata. Также примером ассоциации микроорганизма и растения является симбиоз цианобактерии Anabaena azollae с водным папоротником Azolla.
Синдром мокрой древесины часто наблюдается у деревьев в состоянии стресса, вызванного такими внешними факторами, как сухость, подкисление почвы, избыток азота и т.д. Поскольку этот синдром снижает качество древесины, он приводит к экономическим потерям. Синдром мокрой древесины вызывают аэробные бактерии и бактерии-бродильщики, которые внедряются во внутреннюю часть ствола, где были обломаны ветви, через повреждения корней или морозобойные трещины. Затем микроорганизмы распространяются внутрь ствола в живые ткани, разлагая пектин в срединных пластинках и ситовидных трубках. После этого дерево не способно регулировать поступление воды, его ткани под действием капиллярных сил наполняются водой, и древесина становится мокнущей. Внутри ткани дерева происходит брожение, в результате которого возможно образование у деревьев с твёрдой древесиной (пихта, сосна, дуб) летучих жирных кислот, а у деревьев с мягкой древесиной (ива, тополь) – метана (это более поздняя стадия брожения). Метан накапливается внутри ствола, и давление в нём повышается до нескольких бар. Деревья с такими повреждениями могут жить в течение десятилетий.
Внутри крупных стволов деревьев с отмершей древесиной могут обитать грибы, вызывая её гниение, которое снаружи может быть незаметным долгое временя.
§ 7.8. Факторы патогенности бактерий и защитные механизмы макроорганизма
Термин «патогенность» означает способность микроорганизмов вызывать заболевания. Он состоит из двух греческих слов: pathos – страдание, болезнь и genes – рождающий. Патогенными, т. е. болезнетворными, являются далеко не все бактерии. Поэтому закономерными являются вопросы: как они возникли, чем определяется их патогенность? Однозначного ответа на него дать невозможно, так как патогенность разных бактерий определяется их особыми свойствами. Одним из объяснений происхождения патогенных бактерий служит допущение того факта, что их появление связано с приспособлением к паразитическому существованию и приобретением в связи с этим таких биологических свойств, которые обеспечивают им способность противостоять защитным механизмам макроорганизма. Как уже отмечалось, между микро– и макроорганизмом существуют различные формы симбиоза: мутуализм, комменсализм и паразитизм. Переход от комменсализма к паразитизму вполне логичен. Это положение подтверждает наличие в природе так называемых микробов-двойников. Например, есть микобактерии, патогенные для человека и теплокровных животных, для холоднокровных и растений, и микобактерии непатогенные (например Mycobacterium smegmatis – представитель микрофлоры слизистой оболочки мочеполовых путей человека). Вероятнее всего предположить, что патогенные микобактерии обособились в разные группы в результате адаптации к паразитизму за счет соответствующих организмов. Вместе с тем возбудители таких заболеваний, как ботулизм и столбняк постоянно существуют во внешней среде: естественной средой обитания для них служит почва. Их патогенность для человека и теплокровных животных связана со способностью продуцировать сильнейшие токсины. Однако не ясно, какую роль токсинообразование играет в жизни и экологии этих бактерий.
Существует и другой механизм превращения непатогенных бактерий в патогенные. Он связан с получением первыми дополнительных генов от бактерифагов либо плазмид. Например, дифтерию у человека вызывают только патогенные Corynebacterium diphtheriae, а способность синтезировать дифтерийный экзотоксин они приобретают в результате лизогенной конверсии. Иначе говоря, болезнетворность этих бактерий зависит от передачи им генов токсигенности от особых токсигенных коринефагов. Интегрируясь в хромосому непатогенных коринебактерий, такие фаги привносят в них свои гены, которые и превращают непатогенные коринебактерии в возбудители дифтерии.
В свою очередь, многие варианты диареегенных кишечных палочек возникли в результате приобретения ими плазмид, в составе которых имеются гены, превращающие непатогенную E.coli в патогенную, способную вызывать различные формы эшерихиозов.
Наконец, в природе существуют различные виды бактерий, способных с помощью сенсорно-регуляторных систем перестраивать свой метаболизм в зависимости от того, в каких условиях они существуют – во внешней среде или в организме теплокровных животных. Эти бактерии (легионеллы, иерсинии и др.) получили название сапронозных, так как их естественной средой обитания являются почва и растительные организмы. Однако попадая в организм человека или животных, они изменяют свой метаболизм в сторону, способствующую их размножению и в этих условиях, т. е. при более высокой температуре в живом организме с его механизмами самозащиты.
Патогенность, или способность вызывать заболевание, не является абсолютной. Ее обусловленность находит свое выражение в следующих фактах:
- Патогенность микробов проявляется всегда по отношению к определенному виду или нескольким видам животных или растений. Есть бактерии, патогенные только для человека, есть патогенные только для животных или растений, но есть патогенные и для человека, и для животных (возбудители чумы, бруцеллеза, туляремии и др.).
- Непатогенный в одних условиях (естественных) для макроорганизма возбудитель может стать патогенным в других, измененных условиях. Например, в естественных условиях куры не болеют сибирской язвой, но если температуру их тела искусственно понизить, они ею заболевают.
- Микроорганизмы, являющиеся непатогенными или условно-патогенными для физиологически здоровых организмов, могут стать патогенными при ослаблении их естественной резистентности особенно под влиянием радиационного облучения.
Патогенность – это способность вызывать заболевание – видовое свойство бактерий, присущее виду в целом, но она может проявляться в разной степени у разных представителей данного вида. Поэтому для оценки степени патогенности используют термин «вирулентность».
Патогенность и вирулентность (от лат. virulentus – ядовитый) обозначают одно и то же – способность вызывать заболевание, но под вирулентностью понимают количественную оценку, т. е. меру, степень патогености. Вирулентность может быть усилена (повышена) и ослаблена (понижена). Это достигается разными способами воздействия на соответствующего возбудителя. Но так как все признаки контролируются генами, то фактически получение авирулентных или высоковирулентных штаммов возбудителей сводится к селекции таких вариантов, всегда имеющихся в каждой популяции, т. е. к созданию благоприятных для их отбора условий. Л. Пастер получил вакцину против сибирской язвы путем выращивания ее возбудителей при высокой температуре (42 °С), которая способствовала утрате плазмиды, определяющей патогенность этого возбудителя. Вакцину против бешенства он получил путем селекции штамма вируса бешенства, высоковирулентного для кроликов, но безвредного для человека. А. Себин получил живую вакцину против полиомиелита путем селекции невирулентных вариантов всех трех типов полиовируса.
Для количественного выражения вирулентности микроорганизмов используют следующие методы: определение Dlm и Dl50. Dlm (Dosis letalis minima) – минимальная смертельная доза микроорганизмов или их токсинов, способная вызвать гибель животного за определенный срок – величина относительная, зависит от вида животного. Dlm для кролика, собаки и морской свинки будет различной. Cтатистически наиболее достоверной летальной принято считать дозу (количество микроорганизмов или их токсинов), вызывающую гибель 50 % зараженных животных – Dl50. Она устанавливается на основании статистической обработки полученных результатов по методу Рида и Менча.
Факторы патогенности бактерий. Патогенность бактерий реализуется через три свойства: инфекционносгь, инвазивность и токсигенность (или токсичность).
Инфекционность – это способность возбудителей проникать в организм и вызывать заболевание. Она обусловлена наличием у возбудителей факторов, способствующих его прикреплению к клеткам организма и их колонизации.
Под инвазивностью понимают способность возбудителей преодолевать защитные механизмы организма, размножаться, проникать в его клетки и распространяться в нем. Это свойство также связано с наличием у патогенных микроорганизмов большой группы факторов патогенности, которые наделяют их способностью к внедрению в клетки и размножению в них; факторов, подавляющих фагоцитоз и препятствующих ему; большой группы ферментов «агрессии и защиты».
Токсигенность бактерий обусловлена выработкой ими экзотоксинов.
Токсичность обусловлена наличием эндотоксинов. Экзотоксины и эндотоксины обладают своеобразным действием и вызывают глубокие нарушения жизнедеятельности организма.
Инфекциозные, инвазивные (агрессивные) и токсигенные (токсические) свойства относительно не связаны друг с другом, они по-разному проявляются у разных микроорганизмов. Существуют микроорганизмы, у которых на первый план выходят агрессивные (инвазивные) свойства. К ним относится, например, возбудитель чумы Y.pestis. Хотя бактерии Y.pestis и образуют экзотоксин («мышиный» токсин), однако основными факторами его патогенности служат те, которые подавляют защитные силы организма, обеспечивая быстрое внутриклеточное размножение возбудителя и распространение его по организму.
В то же время возбудители столбняка, дифтерии и ботулизма, обладая слабыми инфекционными свойствами, продуцируют сильнейшие экзотоксины, которые и обусловливают развитие болезни, ее патогенез и клинику.
Следовательно, такое сложное биологическое свойство, как патогенность обусловлено наличием у патогенных бактерий конкретных факторов патогенности, каждый из которых ответственен за проявление конкретных свойств. К ним относятся:
- Хемотаксис и подвижность (у бактерий, имеющих жгутики). С помощью хемотаксиса бактерии ориентируются в отношении своих клеток-мишеней, а наличие жгутиков ускоряет их приближение к клеткам.
- Ферменты, разрушающие субстраты слизи, которая покрывает эпителиальные клетки слизистых оболочек. Протеазы, нейраминидазы, лецитиназы и другие ферменты, разрушая слизь, способствуют высвобождению рецепторов, с которыми взаимодействуют микроорганизмы.
- Факторы адгезии и колонизации, с помощью которых бактерии распознают рецепторы на мембранах клеток, прикрепляются к ним и колонизируют клетки. У бактерий функцию факторов адгезии выполняют различные структуры клеточной стенки: фимбрии, белки наружной мембраны, ЛПС и другие компоненты. Адгезия является пусковым механизмом реализации патогенности. Бактерии могут размножаться, либо в клетках, либо на поверхности клеток слизистой (на их мембранах), либо проходить через них и далее распространяться по организму. Поэтому ни один возбудитель, в том числе и вирусы, не может реализовать свою патогенность, если он не способен прикрепиться к клетке (адсорбироваться на ней). В свою очередь, и токсины, до тех пор, пока они не свяжутся с рецепторами мембран клеток-мишеней, также не смогут реализовать токсические функции. Поэтому адгезия и колонизация являются начальными, пусковыми механизмами развития болезни.
- Факторы инвазии, с помощью которых бактерии проникают в клетку. Обычно они сопряжены с факторами, подавляющими клеточную активность и способствующими внутриклеточному размножению бактерий. Факторы инвазии у грамотрицательных бактерий обычно представлены белками наружной мембраны.
- Факторы, препятствующие фагоцитозу, т. е. защищающие от фагоцитоза. Они также связаны с компонентами клеточной стенки и либо маскируют бактерии от фагоцитов, либо подавляют их активность. Такие факторы есть у многих бактерий. Они представлены либо капсулой из гиалуроновой кислоты, которая не распознается фагоцитами как чужеродная, так как химически не отличается от таковой организма, либо капсулами другой химической природы (у B.anthracis, Y.pestis и т. д.); различными белками, тормозящими фагоцитоз, – белок А (у стафилококков), М–белок (у стрептококков); пленка из фибрина, образующаяся у стафилококков, имеющих плазмокоагулазу; к их числу относятся также пептидогликан, тейхоевые кислоты и другие компоненты клеточной стенки.
- Факторы, подавляющие фагоцитоз, например V–W–антигены у Y.pestis. Наличие таких факторов обусловливает незавершенный характер фагоцитоза. Чаще всего он связан с образованием бактериями веществ, которые подавляют «окислительный взрыв» фагоцитов. Незавершенный фагоцитоз – одна из важных причин хронического течения болезни.
- Ферменты «защиты и агрессии» бактерий. С помощью таких ферментов, как фибринолизин, лецитиназа, гналуронидаза, протеазы и тому подобных бактерии реализуют (наряду с факторами, подавляющими фагоцитоз и защищающими от него) свои агрессивные свойства. Эти ферменты способствуют их распространению в тканях организма. Одним из главных ферментов защиты (например, у стафилококков) является плазмокоагулаза. Превращая фибриноген в фибрин, этот фермент образует своеобразную белковую пленку вокруг клеток, которая и защищает их от фагоцитоза. Патогенность может быть связана и с другими ферментами бактерий, например с аминопептидазами, подавляющими хемотаксис фагоцитов, а также с продуктами жизнедеятельности бактерий, обладающими токсическими свойствами (птомаины и т. п.).
- Токсины микробов. Различают эндотоксины и экзотоксины. Эндотоксины имеются только у грамотрицательных бактерий. Они представлены липополисахаридами и связанными с ними белками. Особенность эндотоксинов в том, что они термостабильны и высвобождаются из бактериальных клеток после их разрушения. Эндотоксины в отличие от экзотоксинов не обладают специфичностью действия. Их токсичность и пирогенность обусловлены липидом А, входящим в состав ЛПС и имеющим сходную структуру у разных грамотрицательных бактерий. Пирогенное действие эндотоксинов не связано с их непосредственным действием на терморегулирующие центры головного мозга. Они индуцируют выброс какого-либо пирогенного вещества из полиморфноядерных лейкоцитов. Эндотоксины являются воспалительными агентами: они увеличивают проницаемость капилляров и оказывают разрушающее действие на клетки. Их воспалительное и пирогенное действие неспецифично. Многообразие проявлений отравления эндотоксином обусловлено не только самим ЛПС, но и высвобождением многочисленных биологически активных соединений, синтез которых он индуцирует в организме человека и животных (гистамин, серотонин, простагландины, лейкотриены и другие, всего более 20). Эти вещества и обусловливают нарушения в различных органах и тканях.
Все три компонента ЛПС – липид А, ядро полисахарида и его боковая цепочка из повторяющихся сахаров – обладают выраженными антигенными свойствами (рис. 4). ЛПС стимулирует синтез интерферонов, активизирует систему комплемента по классическому пути, обладает митогенным действием в отношении лимфоцитов, а также аллергенным действием. Его токсические свойства в отличие от экзотоксинов не снимаются при обработке формалином, и ЛПС не превращается в анатоксин.
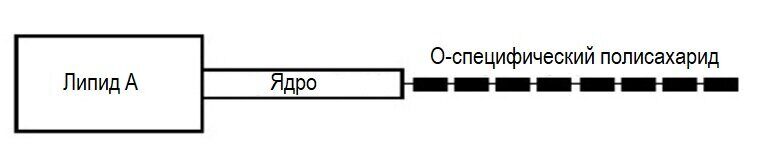
Рис. 4. Схема строения липополисахарида (ЛПС)
Экзотоксины. Их продуцируют как грамположительные, так и грамотрицательные бактерии. У грамположительных бактерий экзотоксины активно секретируются через ЦМ и клеточную стенку в окружающую среду с использованием специальных секретирующих систем. У грамотрицательных бактерий (холерный вибрион, токсигенные кишечные палочки, сальмонеллы) некоторые экзотоксины (энтеротоксины) синтезируются только при определенных условиях непосредственно в инфицированном организме и нередко сохраняются в цитоплазме, освобождаясь из клетки только после ее разрушения.
Основные свойства экзотоксинов. Все известные бактериальные экзотоксины – белки, среди них есть термолабильные и термостабильные. С белковой природой экзотоксинов связаны их основные свойства: они обладают высокой силой действия (самые сильные токсины в природе микробного происхождения), высокой избирательностью и связанной с ней специфичностью действия (картина столбняка у лабораторных животных одинакова как при заражении их возбудителем, так и его экзотоксином), которое они проявляют после некоторого латентного периода. Экзотоксины являются сильными антигенами, а некоторые – даже суперантигенами. Они индуцируют образование в организме антител, т. е. антитоксинов, которые нейтрализуют их действие.
При обработке формалином экзотоксины обезвреживаются и превращаются в анатоксины. Анатоксины лишены токсических свойств, но сохраняют свою способность индуцировать синтез антитоксинов, поэтому широко используются для создания искусственного иммунитета против дифтерии, столбняка, ботулизма и других заболеваний.
По молекулярной организации различают две основные группы экзотоксинов:
- Экзотоксины, состоящие из двух фрагментов – А и В. Каждый фрагмент сам по себе не активен. Свойствами токсина они обладают будучи связанными друг с другом. При этом фрагмент В выполняет две функции – акцепторную (распознает рецептор на мембране и связывается с ним) и формирования внутримембранного канала. Фрагмент А проникает через него в клетку и проявляет в ней токсическую активность, воздействуя на различные процессы метаболизма клетки. Такую структуру имеют, например, энтеротоксины холерного вибриона и патогенных грамотрицательных бактерий.
- «Разрезанные» токсины. Эти экзотоксины синтезируются в бактериальных клетках в виде единой неактивной полипептидной цепи. В активную форму протоксин превращается в результате разрезания его протеазой. Образующийся при этом активный токсин состоит из двух связанных между собой дисульфидными связями пептидных цепей. Активация токсина (разрезание полипептидной цепи) может осуществляться либо собственной бактериальной протеазой, либо протеазами кишечного тракта макроорганизма. Такой тип экзотоксинов синтезируют C.tetani и C.botulinum, причем в их токсинах содержатся дополнительные белки с иными, нетоксическими свойствами.
Вероятно, существуют микробные экзотоксины и с иной химической структурой.
По характеру токсического действия экзотоксины также отличаются друг от друга. Например, экзотоксины с механизмом действия, повреждающим мембраны, разрушают эритроциты, лейкоциты, тромбоциты, базофилы, мастоциты и другие клетки, а также клетки культур тканей, протопласты и сферопласты.
Механизм действия других экзотоксинов связан с повреждением жизненно важных процессов в клетке: подавлением биосинтеза белка (дифтерийный экзотоксин) и переносом электронов по цепи их переноса («мышиный» токсин Y.pestis).
Энтеротоксины холерного вибриона и патогенных грамотрицательных бактерий, воздействуя на аденилатциклазную систему энтероцитов, вызывают выход ионов и воды из тканей в кишечник, что и обусловливает патогенез холеры и других форм диареи. Экзотоксин C.botulinum подавляет выделение ацетилхолина в нервно-мышечном синапсе и блокирует передачу нервного импульса на мышечное волокно. Механизм действия экзотоксина C.tetani также связан с торможением передачи синаптических медиаторов (ацетилхолина, норадреналина и других).
Особым образом проявляют свое действие энтеротоксины, продуцируемые стафилококками. Эти белки обладают свойствами суперантигенов, т. е. антигенов, которые стимулируют синтез излишнего количества Т-лимфоцитов и начинают вырабатывать огромное количество интерлейкина-2, а это и приводит к токсическому эффекту. Таким образом, свое отравляющее действие на организм стафилококковые энтеротоксины реализуют через индуцируемый ими синтез интерлейкина-2.
Особенности генетического контроля синтеза факторов патогенности бактерий. У бактерий обнаружены три типа генов, осуществляющих контроль синтеза факторов патогенности: а) гены собственной хромосомы; б) гены, привнесенные плазмидами; в) гены, привнесенные умеренными конвертирующими фагами. Синтез экзотоксинов и факторов адгезии у энтеротоксигенных штаммов Escherichia coli осуществляется генами, привнесенными Ent-плазмидами. Синтез эксфолиативного токсина типа А у стафилококков контролируется хромосомным геном, а типа В – плазмидным геном; синтез экзотоксина у Corynebacterium diphtheriae – привнесенными tox-генами коринефага.
Дополнительные источники генов патогенности у микроорганизмов, носителями которых являются вирусы и плазмиды, – это один из факторов возникновения патогенных для человека и животных бактерий.
§ 7.9. Основные группы антибиотиков
По направленности своего действия все антибиотики можно разделить на следующие основные группы: 1) противобактериальные; 2) противогрибковые; 3) противовирусные; 4) противоопухолевые. Некоторые авторы относят к антибиотикам не только химические вещества, вырабатываемые мироорганизмами, но и неприродные соединения, которые синтезируют химическими способами, основываясь не на происхождении препарата, а только на его антимикробной активности.
Противобактериальные антибиотики составляют наиболее обширную группу антибактериальных препаратов. К ним относятся:
- Бета-лактамовые антибиотики, которые включают природные пенициллины, несколько поколений полусинтетических пенициллинов (метициллин, оксациллин, ампициллин, карбенициллин, амоксициллин, сулациллин и др.), несколько поколений цефалоспоринов (цефалоридин, цефаметин, цефиксим, цефетамин, цефтриаксон, цефоперазон и др.), нетрадиционные бета-лактамы (карба- и оксапенемы; карба- и оксацефемы и др.). Всего группа бета-лактамных антибиотиков включает в себя около 100 препаратов, активных против многих грамположительных и грамотрицательных, аэробных и анаэробных бактерий.
- Стрептомицины и стрептомициноподобные антибиотики, активные против возбудителей туберкулеза, особо опасных инфекций и ряда грамотрицательных бактерий.
- Манролиды – антибиотики, содержащие в своем составе макроциклическое лактонное кольцо, связанное с углеводными остатками. К этой группе относятся эритромицин, олеандомицин, карбомицин. Макролиды активны в отношении грамположительных бактерий (стафилококки, стрептококки и др.), а также некоторых грамотрицательных бактерий (бруцеллы, холерный вибрион, риккетсии и др.).
- Аминогликозиды – антибиотики олигосахаридной или псевдоолигосахаридной природы: гентамицин, неомшин, канамицин, мономицин, а также тобрамицин, амикацин, сизомицин, нетилмицин. Гентамицин обладает широким спектром действия, подавляет рост многих грамположительных и грамотрицательных бактерий, высокоактивен против псевдомонад, протея. Антимикробные спектры мономицина, неомицина и канамицина близки к спектру гентамицина, но они уступают ему по своей активности.
- Тетрациклины. Основой молекулы этих антибиотиков является полифункциональное соединение – тетрациклин. К этой группе относятся антибиотики с широким спектром действия, активные против многих грамположительных и грамотрицательных бактерий: хлортетрациклин, окситетрациклин, тетрациклин и их производные.
- Гликопептиды – высокомолекулярные соединения, содержащие углеводы и аминокислоты: ванкомицин, ристомицин, линкомицин, клиндамицин, эремомицин и др. Действуют на многие грамположительные кокки и палочки, неактивны в отношении грамотрицательных бактерий. Ванкомицин применяют для лечения псевдомембранозного колита, вызванного Clostridium difficile. Этот колит часто возникает на фоне применения антибиотиков – антибиотикоассоциированный колит.
- Хлорамфеникол (левомицетин) также является антибиотиком широкого спектра действия, активен в отношении многих видов грамотрицательных, включая риккетсии и спирохеты, и грамположительных бактерий. Большинство штаммов бактерий, устойчивых к пенициллинам, стрептомицинам и другим антибиотикам, сохраняет свою чувствительность к левомицетину.
- Противотуберкулезные антибиотики. Противотуберкулезной активностью обладают производные парааминосалициловой кислоты (препараты ПАСК), изоникотиновой кислоты (изониазиды), а также стрептомицин и его производные. Они составляют препараты первого ряда. К противотуберкулезным препаратам второго ряда относятся флоримицин, циклосерин и рифампицины. К рифампицинам высоко чувствительны также стафилококки, стрептококки, грамотрицательные кокки, многие не образующие спор анаэробы, сальмонеллы, возбудители особо опасных инфекций и другие бактерии – внутриклеточные паразиты.
- Фосфомицины – антибиотики из группы фосфоновой кислоты. Фосфомицин обладает сильным бактерицидным действием на грамотрицательные бактерии (Escherichia, Proteus, Pseudomonas, Serratia, Salmonella, Shigella и другие роды).
- Неприродные соединения – фторхинолоны. В клинике уже применяют около десятка фторхинолоновых препаратов (ципрофлоксацин, нефлоксацин, офлоксацин, ципробан и др.). Они обладают бактерицидным действием на многие грамотрицательные бактерии, в том числе на возбудителей самых тяжелых заболеваний. По своей эффективности фторхинолоны не уступают цефалостринам 3-го и 4-го поколений.
Пять групп антибиотиков обладают наиболее широким спектром антимикробного действия: бета-лактамы, фторхинолоны, аминогликозиды, тетрациклины и хлорамфеникол.
К препаратам, обладающим противогрибковым действием, относятся леворин, нистатин, амфтерицин В и некоторые другие полиеновые (содержащие сопряженные двойные связи) антибиотики, также гризеофульвин, низорал, 5-фторцитозин (флуцитозин) – препараты группы имидазолов.
Противовирусные препараты. К этой группе относятся прежде всего интерфероны. Они активны против ДНК- и РНК- содержащих вирусов. Других антибиотиков, которые обладали бы широким противовирусным действием, пока ещё не найдено. Однако синтезированы различные химические соединения, подавляющие размножение некоторых вирусов. Например, амантадин и ремантадин подавляют размножение вирусов ганцикловир – вирусов герпеса; азидотимидин – вируса СПИДа. Жизненный цикл вирусов настолько тесно связан с жизнью клетки, что найти или синтезировать такое химическое вещество, которое избирательно действовало бы только на вирус и не влияло на жизнь клетки, оказалось значительно труднее. Однако поиски таких препаратов интенсивно ведутся.
§ 7.10. Механизм действия антибиотиков
Все антибиотики обладают избирательностью действия. Их относительная безвредность для человека определяется, прежде всего, тем, что они специфически подавляют такие метаболические процессы в микробной клетке или у вируса, которые отсутствуют в эукариотной клетке или недоступны для них. В этом отношении уникальным является механизм действия бета-лактамных антибиотиков. Мишенями для них являются транспептидазы, которые завершают синтез пептидогликана клеточной стенки. Поскольку клеточная стенка есть только у прокариот, в эукариотной клетке нет мишеней для бета-лактамных антибиотиков. Транспептидазы представляют собой набор белков-ферментов, локализованных в цитоплазматической мембране бактериальной клетки. Отдельные бета-лактамы различаются по степени сродства к тому или иному ферменту, которые получили название пенициллинсвязывающих белков. Поэтому биологический эффект бета-лактамных антибиотиков различен – от бактериостатического до бактерицидного, литического.
Кроме бета-лактамных антибиотиков синтез клеточной стенки поражают такие антибиотики, как бацитрацин, фосфомицин, циклосерин, ванкомицин, ристомицин, однако иным путем, чем пенициллин. Все они, кроме циклосерина, вызывают бактерицидный эффект.
Механизм действия таких антибиотиков, как хлорамфеникол, тетрациклины, стрептомицин, аминогликозиды, эритромицин, олеандомицин, и другие макролиды, линкозамиды, фузидиевая кислота, пуромицин связан с угнетением синтеза белка на уровне рибосом 70S. Хотя бактериальные рибосомы 70S имеют такую же в принципе структуру, как рибосомы 80S эукариотных клеток, их белки и белковые факторы, участвующие в работе белоксинтезирующей системы, отличаются от таковых рибосом 80S. Этим и объясняется избирательность действия указанных антибиотиков на белковый синтез бактерий. Разные антибиотики по-разному блокируют синтез белка. Тетрациклины блокируют связывание аминоацил-тРНК на А-участке рибосомы 70S. Хлорамфеникол подавляет пептидилтрансферазную реакцию. Стрептомицины препятствуют превращению инициаторного комплекса в функционально активную рибосому. Эритромицин блокирует реакцию транслокации. Пуромицин, присоединяясь к растущему концу синтезируемой полнопептидной цепи, вызывает преждевременное отделение ее от рибосомы. Механизм действия фторхинолонов связан с их избирательным подавлением бактериальных ферментов ДНК-гираз, участвующих в репликации ДНК. Фторхинолоны связываются со специфическими участками ДНК, которые создаются воздействием ДНК-гиразы, и подавляют ее активность.
Рифампицины угнетают активность ДНК-зависимых РНК-полимераз, вследствие чего у бактерий подавляются процессы транскрипции.
Активность противоопухолевых антибиотиков связана с тем, что они либо являются ингибитором синтеза ДНК (брунеомицин), либо подавляют активность ДНК в системе ДНК-зависимой РНК-полимеразы, т. е. блокируют транскрипцию (антрациклины, актиномицины).
§ 7.11. Лекарственная устойчивость бактерий
Существуют два типа лекарственной устойчивости бактерий - естественная (или природная) и приобретенная.
Естественная лекарственная устойчивость является видовым признаком. Она присуща всем представителям данного вида и не зависит от первичного контакта с данным антибиотиком, в ее основе нет никаких специфических механизмов. Чаще всего эта резистентность связана с недоступностью мишеней для данного антибиотика, обусловленной очень слабой проницаемостью клеточной стенки и цитоплазматической мембраны, или какими-либо другими причинами. Если низкая проницаемость существует к нескольким антибиотикам, то она будет обусловливать полирезистентность таких бактерий.
Приобретенная лекарственная устойчивость возникает у отдельных представителей данного вида бактерий только в результате изменения ее генома. Возможны два варианта генетических изменений. Один из них связан с мутациями в тех или иных генах бактериальной хромосомы, вследствие которых продукт атакуемого гена перестает быть мишенью для данного антибиотика. Это происходит либо вследствие изменения структуры белка, либо потому, что он становится недоступным для антибиотика.
В другом случае бактерии становятся устойчивыми к антибиотику или даже сразу к нескольким антибиотикам благодаря приобретению дополнительных генов, носителями которых являются R-плазмиды. Никаких других механизмов приобретенной лекарственной устойчивости не существует. Однако, приобретая устойчивость к антибиотику, а тем более сразу к нескольким антибиотикам, такие бактерии получают наивыгоднейшие преимущества: благодаря избирательному давлению антибиотиков происходит вытеснение чувствительных к ним штаммов данного вида, а антибиотикоустойчивые варианты выживают и начинают играть главную роль в эпидемиологии данного заболевания. Именно они и становятся источниками формирования тех клонов бактерий, которые обеспечивают эпидемическое распространение возбудителя. Решающую роль в распространении лекарственной устойчивости, в том числе множественной, играют R-плазмиды благодаря их способности к самопереносу.
§ 7.12. Биохимические основы антибиотикорезистентности
Можно выделить следующие пять биохимических механизмов формирования резистентности.
- Разрушение молекулы антибиотика. Такой механизм лежит, главным образом, в основе формирования устойчивости к бета-лактамным антибиотикам. Бета-лактамазы, разрушая структуру пенициллинов и цефалоспоринов, обеспечивают устойчивость бактерий к ним.
- Модификация структуры молекулы антибиотика, в результате которой утрачивается ее биологическая активность. Гены, содержащиеся в R-плазмидах, кодируют белки, которые вызывают различные модификации молекул антибиотика путем их ацетилирования, фосфорилирования или аденилирования. Именно таким путем инактивируются аминогликозиды, макролиды, хлорамфеникол, клиндамицин и другие антибиотики.
- Изменение структуры чувствительных к действию антибиотиков белков. Изменение структуры белков рибосом 70S лежит в основе устойчивости к стрептомицину, аминогликозидам, макролидам, тетрациклинам и другим антибиотикам. Изменение структуры бактериальных гираз в результате мутации приводит к формированию устойчивости к хинолонам; РНК-полимераз – к рифампицину; пенициллинсвязывающих белков (транспептидаз) – к бета-лактамам и т. п.
- Образование бактериями «обходного» пути метаболизма для биосинтеза белка-мишени, который оказывается нечувствительным к данному химиопрепарату, – механизм, который лежит в основе резистентности к сульфаниламидным препаратам.
- Формирование механизма активного выведения из клетки антибиотика, в результате чего он не успевает достичь своей мишени (один из вариантов устойчивости к тетрациклинам).
Необычный механизм устойчивости к изониазиду обнаружен у М.tuberculosis. Действие изониазида на туберкулезную палочку зависит от наличия у последней плазмиды, в составе которой имеется особый ген. Продукт этого гена превращает неактивный изониазид в активную форму, которая разрушает бактериальную клетку. Утрата этого гена обусловливает устойчивость М.tuberculosis к изониазиду.
В некоторых случаях инактивацию антибиотиков, которая лежит в основе резистентности к ним, бактерии могут осуществлять разными механизмами. Так, например, существуют три механизма, ответственных за формирование устойчивости к бета-лактамным антибиотикам: слабая проницаемость наружной мембраны клеточной стенки грамотрицательных бактерий, обеспечивающая природную устойчивость; изменение структуры пенициллинсвязывающих белков в результате мутаций, которое приводит к утрате их сродства к антибиотику; продукция бета-лактамаз, разрушающих антибиотик. Существуют три типа устойчивости и к тетрациклинам, определяемой:
1) выносом тетрациклина из клетки белком цитоплазматической мембраны; 2) изменением структуры белка-мишени рибосом; 3) модификацией тетрациклина в неактивную форму.
Возможно, у бактерий существуют и другие механизмы формирования устойчивости к лекарственным препаратам.
На каждый новый антибиотик бактерии отвечают появлением резистентных к нему штаммов. Поэтому следует предвидеть пути постоянного преодоления этого препятствия.
В природе, особенно в почве, а также в кишечнике человека и животных микроорганизмы сосуществуют в столь тесных взаимоотношениях, что это обеспечивает им постоянную возможность обмена генетическим материалом с помощью различных механизмов, в том числе и с помощью конъюгации. Так как многие гены лекарственной устойчивости несут в себе транспонируемые элементы, то это обеспечивает им возможность к большой мобильности. Они могут перемещаться внутри хромосомы, переходить из хромосом в плазмиды, формировать новые варианты плазмид и подвергаться другим превращениям. Таким образом, обмен генами лекарственной устойчивости между микроорганизмами в естественных условиях вполне возможен, что может приводить к устойчивости микроорганизмов к новым вариантам модифицированного антибиотика.
Способы определения чувствительности (резистентности) бактерий к химиопрепаратам. Существуют различные способы определения чувствительности бактерий к антибиотикам, но чаще всего используются два из них: метод диффузии в агар с применением стандартных дисков, пропитанных антибиотиком, и метод серийных разведений антибиотика.
Первый из них заключается в использовании заранее приготовленных из фильтровального картона дисков диаметром 6 ± 0,5 мм. В России выпускается более 20 стандартных дисков. Содержание антибиотика в диске варьирует в зависимости от его терапевтической дозы и выражается в микрограммах на миллилитр (мкг/мл) или в единицах действия (ЕД). Диски одного наименования содержат одну дозу антибиотика, она составляет: 5 (рифампицин), 6 или 10 мкг/мл (бензилпенициллин) и т.д. Оценка результатов определения чувствительности основана на установлении зависимости размеров зон подавления роста исследуемых культур вокруг дисков с антибиотиками и значениями минимальных подавляющих концентраций (МПК) соответствующих антибиотиков в отношении тех или иных культур. Установление такой зависимости в соответствии с методическими указаниями позволяет придать оценке результатов полуколичественный характер и отнести исследуемые культуры бактерий к одной из трех категорий: устойчивые, умеренно устойчивые, чувствительные.
Более точным является количественный метод, позволяющий определить минимальную подавляющую концентрацию (МПК) антибиотика, выраженную в микрограммах на миллилитр (мкг/мл). С этой целью делают серийные разведения антибиотика и добавляют их в жидкую или плотную питательную среду, а затем определяют, при какой минимальной концентрации антибиотика произошло подавление роста исследуемого штамма возбудителя.
Бактериологические анализаторы. С целью совершенствования методов бактериологической диагностики инфекционных болезней и одновременного определения чувствительности возбудителя к антибиотикам разработаны и широко внедряются в практику различные автоматические и полуавтоматические бактериологические анализаторы, которые позволяют бактериологам избежать рутинной работы, значительно быстрее проводить идентификацию культуры и изучать ее чувствительность к антибактериальным препаратам (рис. 5).

Рис. 5. Бактериологический анализатор VITEK, производитель – фирма «BIOMERIEUX» (Франция): А – автоматический анализатор с поддержанием постоянной температуры и влажности; Б – персональный компьютер с программным обеспечением; В – принтер для распечатки результатов; Г – панели с ячейками, содержащими различные тест-субстраты
В комплект автоматического бактериологического анализатора обычно входят автоматический анализатор с поддержанием постоянной температуры и влажности (А), персональный компьютер с программным обеспечением (Б), принтер для распечатки результатов (В), прибор для стандартизации мутности. Суспензия первично выделенной культуры переносится в панели с ячейками (Г), содержащими различные тест-субстраты (более 30), по которым за короткий срок удается дифференцировать многие виды бактерий по их биохимическим свойствам.
Кроме того, имеются панели с ячейками, содержащими антибиотики (более 40 препаратов в 30 различных комбинациях) (рис. 6). Идентификация и проверка чувствительности к антибиотикам осуществляется за 2 – 3,5 часа спектрофотометрическим и флуоресцентным методами.

Рис. 6. Микробиологический анализатор BIOMIC V3, производитель – «Giles Scientific» (США): А – чашка Петри с культурами бактерий; Б – панели с ячейками, содержащими различные тест-субстраты; В – определение чувствительности к антибиотикам (на экране видны зоны лизиса бактерий вокруг дисков с антибиотиками)
Система VITEK позволяет идентифицировать более 2500 видов микроорганизмов, в том числе грамположительные, грамотрицательные, грибы, анаэробы и другие. Программное обеспечение позволяет выбирать наиболее эффективный лекарственный препарат и контролировать проводимую антибиотикотерапию, сохранять и обрабатывать полученную информацию.
Побочные реакции, наблюдаемые при антибиотикотерапии. Хотя к антибиотикам предъявляются жесткие требования в отношении их безвредности для человека, в некоторых случаях, особенно при неоднократном или длительном применении их, наблюдаются нежелательные реакции, которые можно разделить на следующие четыре группы: аллергические, токсические, эндотоксические и дисбактериозы. Аллергические реакции наблюдаются в тех случаях, когда антибиотик выступает в качестве аллергена. Они не зависят от дозы введенного препарата, могут наступать за первым введением его, но обычно возникают в результате постепенной сенсибилизации при повторных применениях антибиотика, могут носить характер крапивницы, дерматита, сыпи, ринита и т. п. Наибольшую опасность представляет пенициллиновый шок – реакция гиперчувствительности немедленного типа.
Токсические реакции возникают чаще всего в связи с органотропным фармакодинамическим действием антибиотика и при продолжительном лечении. Проявляются в виде поражения вестибулярного аппарата (неомицин, канамицин, стрептомицин и некоторые другие), почек (полимиксин, бацитрацин, неомицин, мономицин, канамицин, стрептомицин и некоторые другие), периферических нервов, различных поражений ЦНС (циклосерин, неомицин, полимиксин, гризеофульвин, пенициллин, стрептомицин и некоторые другие) и других нарушений.
Наиболее тяжелым является токсическое воздействие на кровь: агранулоцитоз, апластическая анемия (левомицетин).
Эндотоксические реакции развиваются в тех случаях, когда под влиянием антибиотика происходит массовое разрушение грамотрицательных бактерий, сопровождающееся выделением и поступлением в кровь их эндотоксина (липополисахарида).
Одним из самых частых осложнений, особенно при длительном применении антибиотиков с широким антимикробным спектром, являются дисбактериозы. Они развиваются в результате того, что применяемый антибиотик действует не только на возбудителя, но и на нормальную микрофлору, угнетая ее. Это ведет к тому, что беспрепятственно начинают размножаться те микроорганизмы, которые к этому антибиотику нечувствительны. Чаще всего это стафилококки, дрожжеподобные грибы Candida, клостридии, некоторые грамотрицательные палочки (псевдомонады, протей и другие). Наиболее тяжело протекают генерализованный кандидоз (кандидосепсис); стафилококковый энтероколит; псевдомембранозный колит, вызываемый C.difficile; вторичные пневмонии, вызываемые стафилококком и грамотрицательными палочками.
Глава 8
МИКРООРГАНИЗМЫ В ГЛОБАЛЬНЫХ БИОГЕОХИМИЧЕСКИХ ЦИКЛАХ
Циклы превращений химических элементов могут быть замкнуты в рамках определенной экосистемы, т. е. не включать обмен промежуточными продуктами между экосистемой и окружающей средой. Но большинство экосистем – это открытые системы, между ними и окружающей средой происходит обмен химическими веществами. Такие экосистемы, как озеро, океан, участок почвы и другие играют роль либо источника химических соединений, либо его акцептора.
Основная роль микроорганизмов в биосфере состоит в минерализации органического вещества, и большинство известных прокариот – гетеротрофы, не смотря на то что автотрофные прокариоты участвуют в образовании значительного количества биомассы на Земле.
§ 8.1. Роль микроорганизмов в круговороте веществ
Превращения химических элементов на Земле в значительной мере определяются биологическими процессами. Микроорганизмы обнаружены повсюду, где есть хотя бы какие-то источники энергии, углерода, азота. В основе разнообразия их метаболизма лежит способность использовать любые, даже самые минимальные возможности для своего существования.
В то же время гигантская роль микроорганизмов в круговороте веществ в природе имеет исключительное значение для сохранения динамического равновесия всей биосферы, нарушение которого может привести к катастрофическим последствиям.
Учёные предполагают, что до появления живых организмов атмосферные газы на нашей планете находились в восстановленном состоянии: углерод – в форме метана (CH4), азот – в форме аммиака (NH3), кислород – в составе воды (H2O). Современное состояние этих химических элементов в виде окисленных форм – углерода в виде оксида (СО2), а азота и кислорода в форме простых газов (N2 и O2) – является следствием в основном активности микроорганизмов.
Газовый состав атмосферы Земли и количественное содержание в ней химических элементов, необходимых для живых организмов, являются результатом равновесия между их образованием и использованием в биологических и геологических процессах.
Автотрофные организмы, в том числе одноклеточные водоросли, и цианобактерии продуцируют органическое вещество из СО2 и других неорганических соединений, а также из воды как источника электронов и выделяют молекулярный кислород (процесс фотосинтеза). Это органическое вещество используется частично самими продуцентами при дыхании и частично животными и человеком (консументами), которые окисляют его до СО2 (потребление). Затем остатки растений и экскременты животных разлагаются микроорганизмами, в первую очередь бактериями и грибами (редуценты): в присутствии кислорода до СО2, в анаэробных условиях до СО2 и метана (биодеградация, минерализация). Азот, сера и фосфор, входящие в состав биомассы, высвобождаются в основном в форме аммиака, сероводорода и фосфата соответственно, затем претерпевают дальнейшие превращения.
Следовательно, основная роль микроорганизмов в биосфере состоит в минерализации органического вещества, и большинство известных прокариот – гетеротрофы.
Другим важным фактором, определяющим роль микроорганизмов в природе, является высокая скорость их размножения при благоприятных условиях.
Автотрофные прокариоты участвуют в первичной (цианобактерии) или вторичной продукции (большинство аноксигенных фототрофных бактерий). Они осуществляют фотосинтез органического вещества, но при этом используют в качестве доноров электронов (Н2S, H2, Fe2+) органические соединения, образование которых обычно связано с трансформацией органических веществ, синтезируемых первичными продуцентами. То же можно сказать и о хемолитотрофных микроорганизмах: они окисляют доноры электронов (например, H2, NH3, H2S, Fe2+ и CO), в большинстве случаев восстановленные при окислении органического вещества, и зависят от восстановителей, действующих как промежуточные носители электронов в процессе разложения органического вещества. Поэтому некорректно считать, что экосистемы в зонах морских гидротермальных вод, которые полностью основаны на первичной продукции хемолитотрофных микроорганизмов, не зависят от фотосинтеза, так как хемосинтезирующие организмы используют в качестве акцептора электронов молекулярный кислород – продукт фото- синтеза, осуществляемого фитопланктоном в поверхностном слое морской воды, наземными растениями и цианобактериями.
Под круговоротом веществ в природе понимают циклические превращения химических элементов, которые входят в состав живых существ. Эти превращения происходят вследствие разнообразия и гибкости метаболизма микроорганизмов. В окружающей среде, по-видимому, нет таких органических веществ, которые не разрушались бы теми или иными микроорганизмами.
Круговороты химических элементов могут замыкаться в границах определенной экосистемы, то есть не включать обмен промежуточными продуктами цикла между экосистемой и окружающей средой. Но большинство экосистем – это открытые системы; между ними и окружающей средой происходит обмен химическими веществами. Такие экосистемы, как озеро, океан, участок почвы выступают как источники или как акцепторы химических соединений, обычно переносимых воздухом или током воды.
Везде и всюду микроорганизмы сосуществуют в виде сложных ассоциаций – биоценозов, представленных многими и разнообразными видами, между которыми складываются своеобразные взаимоотношения.
Особенности этих взаимоотношений таковы, что они обеспечивают существование всех многочисленных видов бактерий и в конечном счете всего царства прокариот, которое, в свою очередь, сосуществует с другими царствами жизни на Земле.
§ 8.2. Круговорот углерода
Углерод является основой всех органических молекул и превалирующим элементом в клеточном (органическом) материале. В его наиболее окисленной форме CO2, он может рассматриваться как неорганическая молекула (сущность органической молекулы – связь С–Н, так, органические формы углерода с эмпирической формулой CH2O являются уменьшенными формами углерода).
Процессы распада безазотистых органических веществ обусловлены по преимуществу жизнедеятельностью микроорганизмов, а процессы созидательные – фотосинтезом зеленых растений, водорослей и фотосинтезирующих бактерий.
Микроорганизмами осуществляется минерализация 90 % органического углерода, то есть превращение его в СО2. Остальные 10 % СО2 образуются в результате дыхания других организмов, а также за счет сгорания топлива и других материалов.
Углеродные ресурсы на Земле составляют шесть основных резервуаров:
- неорганические карбонаты в осадочных породах и осадках;
- органический восстановленный углерод биогенного происхождения в виде ископаемых – каменного угля, природного газа, нефти и осадков;
- карбонаты, бикарбонаты и растворённый СО2 в морской воде;
- органический углерод в составе почвенного гумуса;
- СО2 в атмосфере;
- органический углерод в составе живой и отмершей биомассы.
В круговороте углерода участвуют преимущественно последние четыре резервуара. В действительности это круговорот диоксида углерода, который зависит от фотосинтетической активности наземных и водных растений, в том числе водорослей и микроорганизмов, которые образуют органические соединения на свету, но затем окисляют примерно одну треть связанного углерода при дыхании, в основном ночью. Разность между количеством синтезированного и потреблённого ими органического вещества составляет 60 Пг (Пт – петаграмм; 1 Пт = 1015 г = 109 т) углерода, и эта масса органического вещества служит источником питания для консументов и минерализоторов, которые в конечном итоге возвращают углерод в окисленной форме в атмосферу, замыкая цикл и поддерживая содержание СО2 в биосфере на уровне примерно 0,035 % (об./об.), что эквивалентно 350 млн-1 (объёмное соотношение).
Общую массу живых организмов, в которой происходят превращения углерода, оценивают примерно как 600 Пг органического углерода. Условно установленная продолжительность жизни живых организмов в среднем составляет 25 лет.
Эту биомассу составляют растительные организмы; на консументы и минерализаторы приходится лишь незначительная часть общей живой биомассы – меньше 2 %.
Дополнительно СО2 поступает в атмосферу в количестве примерно 5,5 Пг при сжигании человеком горючих ископаемых – угля, нефти и природного газа.
Эти запасы связанного углерода, накопившегося в ранние геологические эпохи в результате трансформации растительных остатков, составляют свыше 7·107 Пг с учётом биогенного метана, связанного в глубоководных осадках в виде газовых гидратов.
К ископаемым запасам органического углерода соответствует накопленный благодаря фотосинтезу запас О2 в атмосфере, составляющий 107 Пг.
Сжигание горючих ископаемых в качестве топлива – это главная причина медленного, но постоянного возрастания содержания диоксида углерода в атмосфере, которое в начале ХХ в. составляло 300 млн-1, а в конце века приблизилось к 350 млн-1 (объемное соотношение).
Ежегодно зеленые растения потребляют около 60 млрд т углекислого газа (или 20 млрд т углерода), а в атмосфере содержится около 600 млрд т углерода.
В океане фотосинтез и минерализация взаимосвязаны и сбалансированы, и уровень СО2 в морской воде довольно стабилен. Запас СО2 в океанах служит мощным буфером, поддерживающим уровень СО2 в атмосфере вследствие интенсивного обмена углекислотой между атмосферой и океаном. Оценить доли участия аэробного окисления и анаэробных процессов в минерализации углерода можно на основании данных, представленных в табл. 3. Учитывая, что почти у всех животных обмен веществ основан на участии анаэробных бактерий-бродильщиков в их пищеварении, можно предполагать, что от 20 до 50 % всего связанного углерода разлагается вначале анаэробно, и уже продукты этого первичного сбраживания окисляются с участием молекулярного кислорода (рис. 7).
Таблица 3 Количество метана (СН4), выделяемого билогическими объектами в атмосферу за год
|
Источник
|
Выделение СН4, Тг С/г.* в среднем
|
|
Затопляемые природные земли
|
90
|
|
Рисовые поля
|
75
|
|
Жвачные
|
60
|
|
Термиты
|
40
|
|
Места захоронения отходов
|
30
|
|
Океаны
|
8
|
|
Пресные воды
|
4
|
|
В целом
|
307
|
* 1 Тг = 1012 г = 106 т.
В основе процессов распада безазотистых органических веществ лежат различные формы брожения, которые постоянно происходят в природе.
Полный процесс биодеградации (разложения)
|
Полимеры
|
Мономеры (деполимеризации)
|
|
Мономеры
|
Жирные кислоты + СО2 + Н2
|
|
Мономеры + О2
|
CO2 + H2O (аэробное дыхание)
|
Брожение – анаэробное дыхание, при котором микроорганизмы используют выделяющуюся энергию для своей жизнедеятельности.
Спиртовое брожение углеводов вызывают дрожжи (Saccharomyces cerevisiae), некоторые виды бактерий (Sarcina ventriculi) и отдельные представители мукоровых грибов рода Мисоr.
При спиртовом брожении молекула гекеозы распадается на этанол и углекислый газ:
С6Н2О6 → 2СН3СН2ОН + 2СО2 + 27 ккал.
Это уравнение отражает лишь конечный результат. В ходе брожения образуется много промежуточных продуктов – гексозомонофосфат, фруктозодифосфат, фосфотриозы, фосфоглицериновая кислота, фосфопировиноградная кислота, пировиноградная кислота, уксусный альдегид и, наконец, этиловый спирт.

Рис. 7. Круговорот углерода
Спиртовое брожение широко используется в промышленности для производства вина и пива, также в хлебопечении. Для этих целей применяют определенные расы дрожжей в виде чистых культур. Дрожжи для заквашивания теста впервые были использованы около 6000 лет назад Египте, а затем этот способ получения хлеба постепенно распространился по всему свету. Способ перегонки спирта был открыт согласно литературным данным в Китае или арабских странах. Винокуренные заводы в Европе появились в середине VII в. Вначале спирт использовали только для приготовления напитков, а затем в связи с развитием промышленности он стал широко применяться как растворитель и химическое сырье.
При содержании в сбраживаемом растворе более чем 30 % сахара часть его остается неиспользованной, так как при этих условиях образуется до 15 % спирта, а при такой концентрации спирт подавляет жизнедеятельность дрожжей. Поэтому натуральные вина содержат не более 15 % спирта. Главное преимущество чистых культур дрожжей заключается в том, что брожение виноградного сока протекает и заканчивается быстро, а отсутствие посторонней микрофлоры позволяет получать вина хорошего вкуса и аромата (с хорошим букетом). По окончании брожения молодое вино стабилизируют и дают ему созреть. Эти процессы занимают несколько месяцев, а при изготовлении высококачественных красных вин – даже несколько лет. В течение первого года во многих красных винах происходит второе, спонтанное, брожение – яблочно-молочнокислое, которое вызывается рядом молочнокислых бактерий (Pediococcus, Leuconostoc, Lactobacillus). В результате этого яблочная кислота винограда превращается в молочную кислоту и СО2, т. е. дикарбоновая кислота превращается в монокарбоновую, и кислотность вина уменьшается, оно становится высококачественным. Игристые вина типа шампанского подвергают второму спиртовому брожению под давлением, добавляя в них сахар. Образующаяся СО2 газирует вино. Второе брожение вызывается различными винными дрожжами, которые после брожения образуют комки и легко удаляются. Вино типа «Херес» крепят добавлением спирта до 15 % и выдерживают на воздухе; на его поверхности интенсивно размножаются определенные дрожжи, что придает вину специфический вкус. В некоторых районах Франции для приготовления десертных вин виноград заражают грибом Botrytis cinerea, а к виноградному суслу добавляют глюкофильные дрожжи, которые сбраживают глюкозу, но не разрушают более сладкую фруктозу, и получается сладкое десертное вино.
Распространенные в природе дикие расы дрожжей рода Torula часто причиняют вред пищевой промышленности, вызывая помутнение и горький вкус напитков.
Уксуснокислое брожение – это биологический окислительный процесс, при котором с помощью уксуснокислых бактерий спирт окисляется в уксусную кислоту. Если какую-либо жидкость, содержащую небольшое количество спирта (вино, пиво), оставить открытой, то в ней постепенно появляются уксусная кислота и кожистая пленка (уксусная матка) на поверхности. Уксуснокислые бактерии объединены в род Acetobacter, содержащий ряд видов и подвидов.
Этиловый спирт под влиянием уксуснокислых бактерий подвергается окислению, в результате которого вначале образуется уксусный альдегид, а затем уксусная кислота. При использовании специальных рас уксуснокислых бактерий максимальный выход уксуса достигает 14,5 %. Уксуснокислые бактерии превращают ряд многоатомных спиртов в сахар. Одна из таких реакций используется для получения сорбозы из сорбитола. Сорбоза – это промежуточный продукт синтеза аскорбиновой кислоты. Она применяется в качестве суспендирующего агента при изготовлении многих лекарственных препаратов.
Уксуснокислые бактерии могут наносить вред винодельческой и пивоваренной промышленности, вызывая прокисание вина и пива.
Молочнокислое брожение – это широко распространенное биохимическое явление, известное как скисание молока. Под воздействием молочнокислых бактерий (семейство Lactobacillaceae) лактоза расщепляется на составляющие ее гексозы – глюкозу и галактозу, которые затем под действием специфических ферментов превращаются в молочную кислоту. Свертывание молока происходит также вследствие того, что молочная кислота отщепляет кальций от казеина, белок превращается в параказеин и выпадает в осадок. Молочнокислые бактерии широко распространены в природе. Они обнаруживаются в молоке, воздухе, на коже, шерсти, в тонком и толстом кишечнике и представлены большим количеством видов палочковидных и кокковидных бактерий, различающихся не только по морфологии, но и физиологическим свойствам (по использованию различных источников углерода и азота).
Различают две группы возбудителей молочнокислого брожения:
1.) возбудители типичного молочнокислого (гомоферментативного) брожения:
C6Н12О6 → 2СН3СНОНСООН;
2.) возбудители нетипичного (гетероферментативного) молочнокислого брожения:
C6Н12О6 → 2СН3СНОНСООН + СО2 (или СН3СООН).
К первой группе относятся бактерии, которые образуют значительное количество молочной кислоты, превращение сахара в молочную кислоту происходит без образования побочных продуктов (или образуются только их следы).
Образование молочной кислоты происходит быстро и интенсивно, а белки гидролизуются до аминокислот. Представители типичного молочнокислого брожения – Streptococcus lactis, Lactobacillus bulgaricus, Lactobacillus caucasicus, Lactobacillus acidophilus и другие виды (рис. 8).
Рис. 8. Молочнокислые бактерии: А – Lactobacillus acidophilus; Б – Bifidobacterium bifidum
С помощью чистых культур истинных молочнокислых бактерий получают высококачественные сорта молочнокислых продуктов.
Наряду со спиртовым брожением молочнокислое имеет большое значение в пищевой промышленности. Целый ряд молочнокислых, спиртомолочнокислых и кислоовощных продуктов получают благодаря жизнедеятельности молочнокислых бактерий или их комбинации с дрожжами: обыкновенная простокваша – S.lactis, мечниковская простокваша – S.lactis + L.bulgaricus; ацидофильное молоко – L. Acidophilus; кефир – L.caucasicus + S.lactis + дрожжи (Torula) (молочнокислое и спиртовое брожение, содержание спирта до 0,2 %); кумыс – из сырого кобыльего молока – L.bulgaricus + S.lactis + Torula (молочнокислое и спиртовое брожение, содержание молочной кислоты около 1 %, спирта до 2,5 %); йогурт – L.bulgaricus + Streptococcus thermophilus; сыры – первичное молочнокислое брожение при температуре 35 °С – S.lactis или S.cremoris, при температуре 42 °С – различные термофильные молочнокислые бактерии, в основном Lactobacillus.
Получение сливочного масла также связано с микробиологическим процессом, так как вначале происходит молочнокислое брожение молока, вызываемое L.bulgaricus, а затем для отделения жира в процессе сбивания необходимо предварительное скисание сливок, которое вызывают стрептококки молока. Они образуют небольшое количество ацетоина, который спонтанно окисляется до диацетила, обусловливающего вкус и запах масла.
Сметана, творог, квашеная капуста, хлебный квас и другие продукты получают при участии молочнокислых бактерий.
К возбудителям нетипичного (гетероферментативного) молочнокислого брожения относятся E.coli, Enterobacter aerogenes и другие бактерии. Наряду с молочной кислотой (она получается в небольших количествах и медленно) эти бактерии образуют и другие продукты брожения: углекислый газ, водород, уксусную, пропионовую кислоты и другие соединения. Эти бактерии осуществляют более глубокое расщепление белков, вплоть до органических соединений и аммиака. Гетеромолочнокислому брожению принадлежит большая роль при силосовании зеленых кормов (рис. 9).

Рис. 9. Представитель семейства Enterobacteriaceae – Escherichia coli
Факультативные анаэробы, в том числе представители семейства Enterobacteriaceae, образуют при брожении в первую очередь органические кислоты: уксусную, муравьиную, янтарную и молочную, а также этанол, глицерин, ацетоин; 2,3–бутандиол, СО2 и Н2. Основные продукты брожения углеводов, которые вызывают строгие спорообразующие анаэробы, – масляная кислота, бутанол, ацетон, изопропанол, другие органические кислоты и спирт. Процессы брожения используют для промышленного производства некоторых из этих продуктов, например бутандиола.
Маслянокислое брожение также широко встречается в природе. Возбудитель маслянокислого брожения был открыт Л. Пастером. На примере маслянокислого брожения Л. Пастер разработал учение об анаэробах. Типичный представитель бактерий маслянокислого брожения – азотфиксирующий Clostridium pasteurianum. Маслянокислые бактерии в больших количествах встречаются в почве, навозе, на растениях, в молоке, сыре. Многие из них являются анаэробами и относятся к роду Clostridium (рис. 10).

Рис. 10. Бактерии рода Clostridium рerfringens
Маслянокислое брожение – сложный биохимический процесс расщепления углеводов, в ряде случаев жиров и белков на масляную кислоту, углекислоту и воду, при этом образуется много побочных продуктов – уксусная, молочная, пропионовая и другие кислоты.
Из числа других форм брожения чрезвычайно важным является брожение целлюлозы (клетчатки), в которой заложены огромные запасы углерода.
Разложение целлюлозы, которая в количественном отношении представляет один из основных компонентов растительных тканей, осуществляется главным образом высоко-специализированными в отношении питания аэробными и анаэробными микроорганизмами.
Среди аэробных бактерий, расщепляющих целлюлозу, наиболее важны скользящие бактерии рода Cytophaga. Целлюлоза – единственное вещество, которое они могут использовать в качестве источника углерода. Цитофаги быстро растворяют и окисляют целлюлозу.
§ 8.3. Круговорот азота и микробы, участвующие в нем
Запасы азота в природе очень велики. Он входит в состав всех организмов на Земле. Общее содержание его в организмах составляет более 25 млрд т, большое количество азота находится также в почве. Но еще более грандиозен запас азота в атмосфере: над каждым гектаром почвы поднимается столб воздуха, содержащий около 80000 т молекулярного азота. Ежегодно на образование вновь вырастающих растений требуется около 1,5 млрд т азота в форме, доступной для усвоения растениями. Имеющегося в воздухе и почве азота хватило бы для обеспечения урожая, даже при одностороннем использовании, на несколько миллионов лет. Однако растения часто дают низкие урожаи именно из-за недостатка азота в почве. Это объясняется тем, что только небольшая группа азотистых соединений может быть быстро усвоена растениями. Не только свободный азот, но и многие формы связанного азота не могут служить источником азотного питания для растений. Азот, поступающий в виде белковых веществ в почву вместе с остатками растений и животных, совсем не годится для этих целей, он должен быть подвергнут минерализации, а образующийся при этом аммиак должен быть окислен в соли азотистой и азотной кислот. В основе процессов круговорота азота лежат следующие биохимические процессы: гниение белков, разложение мочевины, нитрификация, денитрификация и фиксация атмосферного азота (рис. 11).
Гниение, или аммонификация белков, – микробиологический процесс, при котором под воздействием гнилостных микроорганизмов происходит гидролитическое расщепление белков, поступающих в почву с трупами животных и отмирающими растениями, с образованием промежуточных продуктов (альбумоз, пептонов, амино– и амидокислот), а также дурнопахнущих веществ – индола, сероводорода, меркап- тана, летучих жирных кислот.
Конечным продуктом гидролиза белков и дезаминирования аминокислот является NН3, поэтому этот процесс и называется аммонификацией белка. Таким образом, при гниении происходит минерализация белковых веществ, которая в зависимости от химического состава белков субстрата, вида гнилостных бактерий и условий их жизнедеятельности может быть полной или не доведенной до конца. При полной минерализации белка образуются Н2О, СО2, NH3, H2S и минеральные соли.

Рис. 11. Круговорот азота
При широком доступе кислорода продукты гидролиза белков подвергаются полному окислению, зловонных веществ образуется значительно меньше, чем при анаэробных условиях. Такой процесс называется тлением.
Гниение – преимущественно анаэробный процесс, при котором полного окисления некоторых продуктов, например жирных кислот, не происходит. Гнилостные микробы широко распространены в почве, воде, воздухе, в животных и растительных организмах. Поэтому любой продукт, не защищенный от них, быстро подвергается гниению. Его вызывают как анаэробные, так и аэробные микроорганизмы, причем они могут действовать и преемственно, и одновременно.
Наиболее энергичными возбудителями гниения, сопровождающегося глубоким распадом белка и образованием азотистых и безазотистых соединений (индола, скатола, жирных кислот, NH3, H2, H2S и др.), являются Bacillus mycoides, B.subtilis, B.mesentericus, бактерии семейства Enterobacteriaceae (Proteus, Escherichia и др.), а также Clostridium putrificum, C.sporogenes. Последние два – анаэробы, содержатся в кишечнике и после смерти вызывают зловонное разложение трупов (рис. 12).
Рис. 12. Клетки Bacillus subtilis
Процессы гниения протекают только при наличии условий, благоприятных для жизнедеятельности их возбудителей (влажность, температура и т. п.). В сухой песчаной почве трупы подвергаются мумификации (высушиванию без гниения). Гнилостные процессы происходят и в организме человека, в частности в кишечнике; причиной их являются E.coli и другие микробы. По мнению И. И. Мечникова, продукты гниения (скатол, индол и др.), постоянно образующиеся в организме, вызывают хроническую интоксикацию и являются одной из причин преждевременного старения.
Гнилостные процессы протекают также при газовой гангрене: ткани, омертвевшие под влиянием образуемых возбудителями этой болезни экзотоксинов, заселяются гнилостными аэробными и анаэробными бактериями и подвергаются распаду. Некоторые гнилостные процессы используются в промышленности с полезной целью, например при выработке кожи для отделения от нее шерсти – швицевании.
Исключительное значение процессов гниения заключается в том, что они играют важную роль в естественном самоочищении почвы и воды. Этим пользуются для строительства специальных очистных сооружений (полей ассенизации, орошения и т. п.), для биологической переработки и обезвреживания фекальных нечистот и сточных вод, содержащих много мертвых белковых субстратов. Гниение ведет к обогащению почвы азотистыми продуктами.
Большое количество связанного азота поступает в почву также в виде мочевины (диамида угольной кислоты) – NH2-CO-NH2. Ежегодно люди и животные выделяют ее около 20 млн т. Но мочевина не может быть непосредственно использована в качестве азотного продукта для питания растений. Она подвергается также аммонификации, которую вызывают различные уробактерии. При этом вначале образуется нестойкая углеаммиачная соль, которая далее расщепляется с образованием NH3, СО2 и Н2О. Мочевая кислота, выделяемая в почву птицами и рептилиями, также быстро минералиэуется особыми группами микроорганизмов с образованием NH3 и СО2. Следующим важным этапом круговорота азота, вслед за образованием NH3, является процесс нитрификации, т. е. окисление NH3 вначале в азотистую, а затем в азотную кислоту, соли которых наиболее пригодны для азотного питания растений. Процесс нитрификации вызывается двумя группами открытых С. Н. Виноградским нитрифицирующих бактерий. Нитрозобактерии окисляют NH3 до азотистой кислоты:
2NH3 + О2 → 2HNO2 + 2Н2О,
а нитробактерии окисляют азотистую кислоту в азотную:
2HNO2 + О2 → 2HNО3.
Нитрифицирующие бактерии – строгие аэробы, хемолитотрофы. Энергию окисления они используют для восстановления СО2 в гексозу. Благодаря нитрифицирующим бактериям в почве могут образовываться огромные скопления солей азотной кислоты в виде селитры (в Чили, Перу). Завершая процесс минерализации белковых веществ, нитрифицирующие бактерии играют исключительно важную роль и в процессах самоочищения почвы и воды, и в санитарно-гигиенических устройствах (поля орошения и т. п.). Таким образом, нитрифицирующие бактерии способствуют повышению урожайности почвы благодаря накоплению в ней азотнокислых солей. Однако в почве происходят и противоположные процессы, т.е. процессы денитрификации, или восстановления микроорганизмами солей азотной кислоты в соли азотистой кислоты и в другие простые азотистые соединения, вплоть до свободного азота, который уходит в атмосферу. Способностью восстанавливать нитраты в нитриты обладает большое количество видов бактерий и грибов. Денитрифицирующие бактерии (в частности, некоторые виды Pseudomonas) в анаэробных условиях используют денитрификацию как основную форму дыхания.
Для них соли азотной и азотистой кислот служат источниками азота. Энергию для своей деятельности денитрифицирующие бактерии получают из органических веществ, которыми богата почва. Денитрифицирующие бактерии наносят вред сельскому хозяйству, так как приводят к обеднению почвы минеральным азотом и переходу свободного азота в атмосферу. Особенно энергично процессы денитрификации развиваются в слежавшейся, плохо аэрируемой почве. Однако утрата азота почвой из-за активности денитрифицирующих бактерий компенсируется деятельностью свободноживущих аэробных, анаэробных и клубеньковых азот-фиксирующих бактерий (рис. 13). Более 90 % азота связывают азотфиксирующие бактерии, т. е. на каждый гектар почвы ежегодно от 25 до 300 кг азота привносят только они. Так при активном участии многих видов микроорганизмов происходит непрерывный круговорот азота в природе, который поддерживает существование жизни на Земле (см. рис. 11).

Рис. 13. Клубеньки на корнях бобовых растений (виды бактерий Rhizobium)
§ 8.4. Цикл серы
Сера – составная часть некоторых белков. Одним из конечных продуктов гниения белков является H2S. Сероводород не усваивается высшими растениями. Биохимические превращения серы восстановительного и окислительного порядка осуществляются пурпурными и зелеными серобактериями. Для них H2S является источником энергии.
Серобактерии окисляют H2S с выделением свободной серы, которая отлагается у них в цитоплазме в виде капель:
2H2S + О2 → 2Н2О + 2S + 41 ккал.
В клетках бактерий сера окисляется далее до серной кислоты:
2S + 2H2O +3O2→2H2SO4 + 118 ккал
Образующиеся сульфаты (соли H2SO4) служат прекрасным питательным веществом для высших растений. H2S в серную кислоту окисляют различные виды пурпурных серобактерий:
H2S + 2Н2О + 2СО2 энергия света→ 2(СН2О) + H2SO4
Наряду с такими сульфурирующими бактериями в природе не менее широко распространены и десульфурирующие микробы (аналоги денитрифицирующих бактерий), они восстановливают сульфа- ты, вызывая образование H2S. Выделение H2S десульфурирующими бактериями происходит в глубинах морей, поэтому в Черном море на глубине 2500 м содержание H2S доходит до 6,5 мл в 1 л воды. Значительное накопление H2S в результате биологического восстановления серы наблюдается в целебных грязях, лиманах и других водоемах.
В санитарном отношении серобактерии являются важными агентами начальной стадии биологического очищения сточных вод и разложения органических отбросов, содержащих серу. Большинство серобактерий принадлежит к родам Thiobacillus, Sulfolobus и Thiospira. Общая схема круговорота серы представлена на рис. 14. Кроме биологического круговорота серы, в атмосфере происходят небиологические превращения ее газообразных форм. Согласно некоторым подсчетам в атмосферу ежегодно выделяется около 90 млн т серы в виде H2S, образующегося биологическим путем. Кроме того, еще 50 млн т поступает в атмосферу в виде SО2, образующейся при сжигании топлива, и около 0,7 млн т в форме H2S и SO2, возникающих в результате действия вулканов. В атмосфере H2S быстро окисляется до SО2 атомарным (О) и молекулярным (О2) кислородом или озоном (О3). SО2 может растворяться в воде с образованием H2SО3 или окисляться медленно до SO4, которая при растворении в воде превращается в H2SO4. Основная масса Н2SО4 вместе с неокисленной H2SО3 возвращается на землю в форме кислоты, которая становится причиной разрушения различных каменных строений, в том числе многих каменных скульптур.

Рис. 14. Круговорот серы
§ 8.5. Круговорот фосфора
С химической стороны круговорот фосфора достаточно прост, поскольку он встречается в живых организмах только в пятивалентном состоянии в виде свободных фосфатных ионов (РО4-3) или в составе органических фосфатных компонентов клетки. Бактерии не способны поглощать большинство органических фосфорсодержащих соединений, свои потребности в фосфоре они удовлетворяют путем поглощения фосфатных ионов, из которых затем синтезируют органические фосфатные соединения. При разложении гнилостными бактериями белковых веществ одновременно с минерализацией азота происходит превращение органического фосфора в фосфатные ионы. По-скольку большая часть фосфатов, несмотря на быстрый круговорот фосфора, находится в виде нерастворимых солей кальция, железа или алюминия, фосфаты также служат фактором, ограничивающим рост растений. Растворимые фосфаты постоянно переносятся из почвы в море вследствие выщелачивания. Этот перенос имеет однонаправленный характер. Лишь небольшая часть фосфатов возвращается на сушу, главным образом в виде отложений гуано морскими птицами. Поэтому доступность фосфатов для растений зависит от непрерывного перевода в раствор нерастворимых фосфатных отложений – процесса, в котором важную роль играют микроорганизмы. Образуемые ими кислые продукты метаболизма (органические кислоты, а также азотная и серная) растворяют фосфат кальция, а образуемый ими H2S способствует растворению фосфата железа.
§ 8.6. Круговорот железа
В круговороте в природе железа большую роль играют железо-бактерии, для которых оно служит источником окислительного дыхания (донором электронов). Железобактерии окисляют закисные соединения в окисные, а освобождающуюся энергию используют для усвоения углерода или карбонатов. Окисление протекает по формуле
4Fе(НСО3)2 + 6Н2О + О2 = 4Fe(OH)3 + 4Н2СО3 + 4СО2.
Из железобактерий лучше других изучена не образующая спор подвижная палочка Thiobacillus ferroxidans, которая окисляет также и серу. К железобактериям относятся некоторые нитчатые бактерии из рода Leptothrix, а также Gallionella, состоящая из спиральных, закрученных в виде пучков тонких (0,01 – 0,3 мкм) нитей, образующих стебелек, на поверхности которого откладывается гидрат окиси железа. Нитчатые железобактерии в водоемах прикрепляются к различным подводным предметам. Нити бактерий «одеты» слизистым чехлом, который пропитывается гидратом окиси железа. Размножаясь в некоторых озерах в огромных количествах, железобактерии образуют накопления железной руды (например в Карелии). При размножении в водопроводах железобактерии могут вызывать закупорку просвета труб.
Этапы круговорота различных элементов осуществляются микроорганизмами разных групп. Непрерывное существование каждой отдельной группы зависит от химических превращений элементов, осуществляемых другими группами микроорганизмов. Разрыв цикла в какой-либо одной точке привел бы к прекращению жизни на Земле. Жизнь непрерывна на Земле потому, что все основные элементы, необходимые для ее проявления (С, N, Н, О, Р, S), подвергаются циклическим превращениям во многом благодаря деятельности микроорганизмов.
§ 8.7. Экология слоистого (напластованного) озера
Роль прокариот в глобальных круговоротах химических элементов, раскрытую в предыдущих главах, можно показать на примере изменения условий обитания живых организмов в разных слоях воды в озере (рис. 15).

Рис. 15. Экология напластованного озера
Поверхность озера хорошо освещается солнцем и насыщена кислородом. Под поверхностным слоем находится зона восстановления нитрата, ниже – зона восстановления железа и марганца, ещё ниже – зона образования сульфида и метана. Это пространственное распределение отражает порядок протекания реакций; альтернативные окислители проникают путём молекулярной диффузии в осадки из толщи воды с примерно одинаковыми скоростями и потребляются внутри осадков в последовательности, представленной выше.
Дно озера и его отложения находятся в темноте, и живые организмы испытывают дефицит кислорода. Обычно мало кислорода и солнечного света проникает сквозь толщу воды с поверхности озера. Предполагая, что источники питания стабильны и не происходит смешивания слоёв воды в озере, можно считать его стабильной экосистемой с рециркуляцией основных химических элементов среди живых систем.
На поверхности озера изобилие солнечного света и O2, CO2 фиксируется и O2 продуцируется. Фотосинтезирующие растения, водоросли и цианобактерии образуют O2, цианобактерии могут даже фиксировать N2; т. е. здесь имеются условия для жизнедеятельности для аэробных бактериий, насекомых и растений.
На дне озера и в донных отложениях в условиях отсутствия солнечного света и кислорода обитают ферментирующие бактерии, которые образуют жирные кислоты, H2 и CO2. Продукты жизнедеятельности этих бактерий используются метаногенами для образования CH4. Анаэробно дышащие бактерии используют NO3 и SO4 в качестве акцепторов электронов, образуя при этом NH3 и H2S. Образующиеся газы H2, CO2, CH4, NH3 и H2S растворяются в воде.
Биологическая активность на поверхности и на дне озера определяет ситуацию в среднем слое воды озера, особенно около раздела аэробных и анаэробных зон. Эта область является биологически очень активной. Здесь осуществляется бактериальный фотосинтез анаэробными бактериями, использующими более длинные волны солнечного света, которые проникают через толщу воды и не поглощаются растениями, находящимися ближе к поверхности озера.
Метанотрофные бактерии остаются только в пределах аэробной области, в которую из донных отложений поднимается метан (CH4), являющийся для них источником углерода, а образующаяся CO2 возвращается в воду. Литотрофные бактерии используют для своей жизнедеятельности азот, серу, NH3 и H2S из донных отложений и выделяют в воду озера NO3 и SO4.
Пространственное распределение окислительно-восстановительных процессов формируется в зависимости от скоростей реакций и скоростей диффузии их продуктов и определяется кинетикой поглощения субстратов в разнообразных метаболитических нишах.
Глава 9
ВЗАИМОДЕЙСТВИЕ МИКРООРГАНИЗМОВ С АБИОТИЧЕСКИМИ ФАКТОРАМИ ОКРУЖАЮЩЕЙ СРЕДЫ
Жизнедеятельность микроорганизмов находится в зависимости от факторов окружающей среды, которые могут оказывать бактерицидное, т.е. уничтожающее, действие на клетки или бактериостатическое, подавляющее размножение микроорганизмов. Мутагенное действие приводит к изменению наследственных свойств. Физические, химические и биологические факторы окружающей среды оказывают различное воздействие на микроорганизмы.
§ 9.1. Влияние физических факторов на микроорганизмы
Различные группы микроорганизмов развиваются при определенных диапазонах температур. Бактерии, растущие при низкой температуре, называют психрофилами, при средней (около 37 °С) – мезофилами, при высокой – термофилами.
К психрофильным микроорганизмам относится большая группа сапрофитов – обитателей почвы, морей, пресных водоемов и сточных вод (железобактерии, псевдомонады, светящиеся бактерии, бациллы). Некоторые из них могут вызывать порчу продуктов питания на холоде. Способностью расти при низких температурах обладают и некоторые патогенные бактерии (возбудитель псевдотуберкулеза размножается при температуре 4 °С). В зависимости от температуры культивирования свойства бактерий меняются. Так, Serratia marcescens образуют при температуре 20 – 25 °С большее количество красного пигмента (продигиозана), чем при температуре 37 °С. Синтез полисахаридов, в том числе капсульных, активируется при более низких температурах культивирования. Интервал температур, при котором возможен рост психрофильных бактерий, колеблется от -10 до 40 °С, а температурный оптимум – от 15 до 40 °С, приближаясь к температурному оптимуму мезофильных бактерий.
Мезофилы включают основную группу патогенных и условно-патогенных бактерий. Они растут в диапазоне температур 10 – 47 °С; оптимум роста для большинства из них – 37 °С.
При более высоких температурах (от 40 до 90 °С) развиваются термофильные бактерии. На дне океана в горячих сульфидных водах живут бактерии, развивающиеся при температуре 250 – 300 °С и давлении 262 атм. Термофилы обитают в горячих источниках, участвуют в процессах самонагревания навоза, зерна, сена. Наличие большого количества термофилов в почве свидетельствует о ее загрязненности навозом и компостом. Поскольку навоз наиболее богат термофилами, их рассматривают как показатель загрязненности почвы.
Температурный фактор учитывают при проведении стерилизации. Вегетативные формы бактерий погибают при температуре 60 °С в течение 20 – 30 мин; споры – в автоклаве при 120 °С под давлением пара.
Хорошо выдерживают микроорганизмы действие низких температур. Поэтому их можно долго хранить в замороженном состоянии, при температуре жидкого газа (–173 °С).
Высушивание. Обезвоживание вызывает нарушение функций большинства микроорганизмов. Наиболее чувствительны к высушиванию патогенные микроорганизмы (возбудители гонореи, менингита, холеры, брюшного тифа, дизентерии и др.). Более устойчивы микроорганизмы, защищенные слизью мокроты. Так, бактерии туберкулеза в мокроте выдерживают высушивание до 90 дней. Устойчивы к высушиванию некоторые капсуло- и слизеобразующие бактерии, но особой устойчивостью обладают споры бактерий.
Высушивание под вакуумом из замороженного состояния – лиофилизацию – используют для продления жизнеспособности, консервирования микроорганизмов. Лиофилизированные культуры микроорганизмов и иммунобиологические препараты длительно (в течение нескольких лет) сохраняются, не изменяя своих первоначальных свойств.
Действие излучения. Неионизирующее излучение – ультрафиолетовые и инфракрасные лучи солнечного света, а также ионизирующее излучение – гамма–излучение радиоактивных веществ и электроны высоких энергий – губительно действуют на микроорганизмы через короткий промежуток времени. УФ-лучи применяют для обеззараживания воздуха и различных предметов в больницах, родильных домах, микробиологических лабораториях. С этой целью используют бактерицидные лампы УФ-излучения с длиной волны 200 – 450 нм.
Ионизирующее излучение применяют для стерилизации одноразовой пластиковой микробиологической посуды, питательных сред, перевязочных материалов, лекарственных препаратов и др. Однако имеются бактерии, устойчивые к действию ионизирующих излучений, например, Micrococcus radiodurans была выделена из ядерного реактора.
§ 9.2. Действие химических веществ
Химические вещества могут оказывать различное действие на микроорганизмы: служить источниками питания; не оказывать какого-либо влияния; стимулировать или подавлять рост. Химические вещества, уничтожающие микроорганизмы в окружающей среде, называются дезинфицирующими. Процесс уничтожения микроорганизмов в окружающей среде называется дезинфекцией. Антимикробные химические вещества могут обладать бактерицидным, вирулицидным, фунгицидным действием и т.д.
Химические вещества, используемые для дезинфекции, относятся к различным группам, среди которых наиболее широко представлены вещества, относящиеся к хлор-, йод- и бромсодержащим соединениям и окислителям. В хлорсодержащих препаратах бактерицидным действием обладает хлор. К этим препаратам относят хлорную известь, хлорамины, пантоцид, неопантоцид, натрия гипохлорит, гипохлорит кальция, дезам, хлордезин, сульфохлорантин и др. Перспективными антимикробными препаратами на основе йода и брома считаются йодопирин и дибромантин. Интенсивными окислителями являются перекись водорода, калия перманганат и др. Они оказывают выраженное бактерицидное действие.
К фенолам и их производным относят фенол, лизол, лизоид, креозот, креолин, хлор-b-нафтол и гексахлорофен.
Выпускаются также бактерицидные мыла (феноловое, дегтярное, зеленое медицинское), которые содержат 3 – 5 % гексахлорофена и обладают наилучшими бактерицидными свойствами.
Антимикробным действием обладают также кислоты и их соли (оксолиновая, салициловая, борная); щелочи (аммиак и его соли, бура); спирты (70 – 80%-ный этанол и др.); альдегиды (формальдегид, b-пропиолактон).
Перспективная группа дезинфицирующих веществ – поверхностно-активные вещества, относящиеся к четвертичным соединениям и амфолитам, обладающие бактерицидными, моющими свойствами и низкой токсичностью (ниртан, амфолан и др.).
Для дезинфекции точных приборов (например, на космических кораблях), а также оборудования и аппаратуры используют газовую смесь из оксида этилена с метилбромидом. Дезинфекцию проводят в герметических условиях.
Глава 10
МИКРООРГАНИЗМЫ В СЕЛЬСКОМ ХОЗЯЙСТВЕ
Прокариоты играют огромную роль в сельском хозяйстве, так как они участвуют в биогехимических циклах важнейших химических элементов, поддерживают плодородие и структуру почв, взаимодействуют с растениями.
Прокариоты составляют наибольшую фракцию почвенной микробной биомассы (от 450 до 7000 кг/га при массе пахотного слоя почвы на площади 1 га 2400 – 2700 т). Распределение микроорганизмов в почве неравномерно, потому что они образуют микроколонии, прикрепляясь к частицам минеральных или органических субстратов. В некоторых почвах плотность бактерий может достигать 108 колониеобразующих единиц (КОЕ) на 1 г сухой почвы.
В конце ХХ в. для повышения урожайности культур и плодородия почв в сельском хозяйстве стали применять живые чистые культуры микроорганизмов в качестве инокулянтов. С каждым годом использование бактериальных инокулянтов увеличивается на значительных площадях, и их роль будет возрастать в особых системах землепользования, таких как рациональное сельское хозяйство или биологическое земледелие, в мероприятиях по очистке почв от загрязнений и восстановлению ландшафтов. В качестве инокулянтов будут созваться новые генетически модифицированные штаммы и, естественно, разрабатываться методы контроля за ними.
§ 10.1. Использование бактерий в качестве биоудобрений
Биоудобрениями называют вносимые в почву микробные инокуляты, заменяющие химические удобрения. В качестве биоудобрений используют свободноживущих, обитающих в ассоциациях или симбиотические азотфиксирующие прокариоты и эукариотические микроорганизмы, например микоризные грибы. Грибы обеспечивают доступность фосфатов, а азотфиксирующие бактерии – азота. Способность восстанавливать молекулярный азот (N2) до аммиака (NH3) встречается у многих бактерий и архей, но немногие виды бактерий образуют симбиозы с высшими растениями, обеспечивая их азотом.
Клубеньковые бактерии фиксируют азот только в условиях симбиоза с бобовыми растениями (см. рис. 13, 16). Для симбиоза между бактериями семейства Rhizobiaceae и бобовыми растениями (семейства Fabaceae) характерно образование специализированных органов (обычно на корнях растений) – клубеньков. Клубеньковые бактерии (род Rhizobium) фиксируют азот из атмосферы с образованием аммиака, большая часть которого усваивается растением. Формирование симбиоза – сложный процесс, который включает последовательность высокоспецифичных сигналов, обеспечивающих взаимодействие только определённых видов Rhizobium с определёнными видами бобовых растений. Более 100 сельскохозяйственных растений, таких как горох, соя, бобы, люцерна, клевер и другие фиксируют азот со скоростью 100 кг на 1 га в год. При интенсивном земледелии скорость может достигать 300 – 600 кг на 1 га в год. То есть симбиоз бактерий Rhizobium и бобовых растений является наиболее важным для земледелия биологическим механизмом поступления азота в почву и затем в растения (табл. 4).
Рис. 16. Часть разрушенного корня растения, на котором видны четыре клетки, содержащие колонии бактерий Rhizobium: n – ядро двух клеток корня; CW – клеточная стенка, которая отделяет две клетки растения. Бактерии находятся в группах, прилегающих к мембранам, и отделены от цитоплазмы клеток растения
Таблица 4 Виды бактерий Rhizobium и растения-хозяина
|
№
п/п
|
Род или вид бактерий
|
Название растения-хозяина
|
|
|
латинское
|
русское
|
||
|
1
|
Rhizobium leguminosarum
биовар viciae
|
Pisum, lens, Vicia
|
Горох, чечевица, вика
|
|
2
|
|||
|
3
|
биовар phaseoli
|
Phaseolus
|
Фасоль
|
|
4
|
биовар trifolii
|
Trifolium
|
Клевер
|
|
5
|
Rhizobium meliloti
|
Medicago, Melilotus,
Trigonella
|
Люцерна, донник
пажитник
|
|
6
|
Rhizobium loti
|
Lotus
|
Лядвенец
|
|
7
|
Rhizobium spp.
|
Acacia
|
Акация
|
|
8
|
Bradyrhizobium japonicum
|
Glycine
|
Соя
|
|
9
|
Bradyrhizobium spp.
|
Vigna, Arachis
|
Вигна, арахис
|
|
10
|
Azorhizobium caulinodans
|
Sesbania
|
Стеблевые и
корневые клубеньки, сесбания
|
|
11
|
Sinorhizobium fredii
|
Glycine
|
Соя
|
Бактерии Rhizobium инфицируют центральные ткани растений, проникая в них по инфекционным нитям, из которых затем внедряются в цитоплазму растительных клеток, где происходит их деление и дифференцировка в азотфиксирующие бактероиды. Бактероиды отделены от цитоплазмы растительных клеток перибактериальной мембраной растительного происхождения.
В зрелом клубеньке клетки растения полностью заполнены бактероидами, которые получают от растения питательные вещества, об- разующиеся при фотосинтезе в листьях. Бактероиды же обеспечивают растение связанным азотом в форме аммиака. Со временем клубеньки стареют, и бактероиды и клетки растения подвергаются процессам деградации.
Строение и физиологические характеристики клубенька обеспечивают поддержание в нём низкой концентрации кислорода. Доказано, что существует физический барьер для диффузии кислорода из наружных слоёв клубенька. Этот барьер и высокая дыхательная активность бактероидов приводят к снижению концентрации кислорода внутри клубенька до 30 нМ, в то время как вне клубенька она составляет 250 нМ. Для обеспечения бактероидов достаточным количеством кислорода растение до начала азотфиксации синтезирует специальный белок – леггемоглобин, который обладает высоким сродством к кислороду.
Актиномицеты рода Frankia образуют внутриклеточные азот-фиксирующие симбиозы со многими (свыше 200 видов из 8 семейств) покрытосеменными растениями тоже в форме корневых клубеньков. Наиболее хорошо изучена ассоциация актиномицетов Frankia с ольхой (род Alnus), при которой образуются многолетние клубеньки коралловидной структуры. Их называют актиноризой. В отличие от клубеньков бобовых растений, актинориза представляет собой модифицированные боковые корни, иногда значительных размеров с дихотомическим ветвлением, которые характеризуются наличием центрального сосудистого пучка. Клетки Frankia проникают в корни ольхи через корневые волоски и индуцируют в гиподерме и кортексе деление клеток, образующих зачаток клубенька. Затем клубенёк развивается как боковой корень. Актиномицеты образуют вегетативные гифы диаметром 0,5 – 1,5 мкм, которые, разрастаясь, проникают в клетки тканей клубенька. При фиксации азота возникают специализированные структуры – везикулы, их диаметр 4 – 6 мкм. Для зрелых азотфиксирующих везикул характерна слоистая оболочка, которая отделяет симбионтов от цитоплазмы клеток растения-хозяина. Эта оболочка содержит гопаноидные липиды, которые могут образовывать многочисленные липидные слои вокруг везикулы. Количество слоёв коррелирует с концентрацией кислорода в окружающей среде. Вероятно, эти слои функционируют как барьер для диффузии кислорода, чтобы обеспечить его низкую концентрацию, необходимую для синтеза фермента нитрогеназы.
Растения, образующие симбиоз с актиномицетами рода Frankia, распространены по всему земному шару, и фиксация азота актиноризой вносит существенный вклад в обогащение почвы азотом.
Интенсивность фиксации азота с участием Frankia варьирует в пределах сопоставимых с таковой у клубеньковых бактерий, составляя 40 – 350 кг на 1 га в год. Поскольку растения-хозяева Frankia широко распространены от Арктики до тропиков, фиксацию азота актиноризами можно считать важным фактором обогащения почвы азотом.
Азотфиксирующие образуют ассоциации с различными эукариотическими организмами, в том числе с высшими растениями (голосеменными, покрытосеменными, папоротниками, печеночниками, антоцеровыми). Из покрытосеменных с азотфиксирующими цианобактериями (Nostoc) образуют симбиоз только представители рода Gunnera. Нити Nostoc проникают в их стебли через специальные железы и обитают внутриклеточно. В других случаях симбиоза Nostoc с растениями цианобактерии локализуются внеклеточно. У голосеменных (Cycadaceae) цианобактерии заселяют коралловидные корни. С папоротниками Azolla нитчатые цианобактерии образуют симбиоз в специальных полостях листьев. Водные папоротники Azolla, плавающие на поверхности воды, имеют ветви, которые несут очерёдные двулопастные листья. Каждый лист имеет спинную воздушную, содержащую хлорофилл и брюшную, погружённую в воду лопасти. В верхней лопасти имеются специальные полости, в которых находятся нитчатые цианобактерии. При разрушении этих полостей цианобактерии высвобождаются в слизистом матриксе, богатом аминокислотами и полисахаридами. Среди ассоциированных бактерий из полостей листьев папоротников Azolla выделяют различные виды бактерий рода Arthrobacter. На основании этого предполагают, что имеет место трёхкомпонентный симбиоз (папоротник Azolla, цианобактерии и бактерий рода Arthrobacter), т. е. более сложный, чем считалось ранее.
Водные папоротники Azolla широко распространены по всему земному шару, но в большом количестве встречаются в тёплых водах в тропическом и субтропическом поясах. Их широко используют в сельском хозяйстве на корм домашним животным и как зелёное удобрение преимущественно при выращивании риса, потому что они быстро разрастаются в прохладных слабо аэрируемых водах, образуя плотную поверхностную плёнку, которая препятствует росту сорной растительности и размножению насекомых. Уровень фиксации азота при симбиозе Azolla/Anabaena варьирует в зависимости от времени года и условий обитания, составляя в среднем 50 – 100 кг азота на 1 га в год.
§ 10.2. Микроорганизмы, вызывающие болезни растений
Болезни растений, вызываемые бактериями, наносят меньший экономический ущерб, чем болезни, вызываемые грибами и вирусами, но они также могут быть причиной больших потерь урожая в поле и при хранении, например бактериальные болезни увядания картофеля, томата и других сельскохозяйственных культур. Бактерии поражают такие культуры, как рис, пшеница, соя и др. В табл. 5 приведены важные болезни растений и фитопатогенные бактерии, вызывающие их.
Некоторые штаммы бактерий родов Pseudomonas, Xanthomonas, Erwinia, Соrynebacterium и Streptomyces заражают и колонизируют растительные ткани, нанося вред растению-хозяину.
Таблица 5 Экономически важные бактериальные болезни растений
|
Симптом
|
Болезнь
|
Возбудитель
|
|
Пятнистость и ожёг
|
|
|
|
Cосудистое
увядание
(вертициллёз)
|
|
|
|
Мягкая гниль
|
|
|
|
Рак
|
|
|
|
Галл
|
|
|
Фитопатогенные бактерии рода Agrobacterium обладают способностью модифицировать геном растения-хозяина, перенося в него фрагмент своей ДНК (Т–ДНК). Такая модификация приводит к неконтролируемому делению клеток растения-хозяина. Т-ДНК-системы бактерий A. tumefaciens и A. rhizogenes представляют естественный механизм переноса генов между прокариотами и высшими растениями, и поэтому они используются в генетической инженерии для создания трансгенных растений.
§ 10.3. Микроорганизмы, способствующие росту и устойчивости растений
Очень многие почвенные микроорганизмы стимулируют рост растений и способствуют повышению урожайности сельскохозяйственных культур по причине того, что они выделяют одно или несколько веществ, действующих на растения как стимулятор роста. Бактерии, ускоряющие рост растений, называют фитостимуляторами.
Положительное влияние на рост растений оказывают бактерии, которые выделяют вещества, подавляющие рост фитопатогенных бактерий.
К бактериям-фитостимуляторам относятся разнообразные микроорганизмы, способные продуцировать одно или несколько веществ, стимулирующих рост растений. Наиболее подробно изучены ризоценозы с участием пяти видов Azospirillum: A.amazonense, A.brasiliense, A.halopraefaerens, A.irakense и A.lipoferum. Эти бактерии в зависимости от почвенно-климатических условий могут заселять ризосферу растений или проникать в корень, оставаясь в межклеточных пространствах (эндоризосфере). Плотность бактерий может достигать 105 – 108 КОЕ на 1 г высушенных корней.
Глава 11
ПЕРСПЕКТИВЫ ПРОМЫШЛЕННОГО ИСПОЛЬЗОВАНИЯ ПРОКАРИОТ, ВОЗМОЖНЫЙ РИСК ПРИМЕНЕНИЯ ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫХ ОРГАНИЗМОВ И ПУТИ ЕГО ПРЕОДОЛЕНИЯ
В течение тысячелетий люди используют микроорганизмы для получения пищевых продуктов, но до XIX в. их роль в этих процессах не была ясна. Многие десятилетия уже после появления работ выдающихся микробиологов Л. Пастера, Р. Коха и других микробиология оставалась описательной наукой.
И только после установления роли ДНК как носителя генетической информации началась новая эра в развитии микробиологии и биотехнологии.
Развитие молекулярной биологии и молекулярной генетики привело к разработке методов генетической инженерии, которые позволили найти способы получения штаммов-продуцентов.
§ 11.1. Конструирование новых штаммов бактерий-суперпродуцентов
Новые микробные штаммы конструируют для промышленного применения с целью придать им способность к росту на простых и дешёвых питательных средах с высокой продуктивностью.
До появления генетической инженерии новые штаммы получали на основе метода ненаправленного мутагенеза и последующего отбора мутантов по определённым признакам, т. е. методом проб и ошибок. Это требовало больших затрат времени и средств, не позволяя осуществлять направленное изменение свойств организма. Кроме того, «избыточный» мутагенез иногда приводит к нестабильности штаммов в результате метаболического дисбаланса. Преимущество и популярность этого метода состоят в том, что он практически не требует сведений о генетике и метаболизме изменяемого штамма и о свойствах продуцируемого штаммом продукта.
Посредством методов генетической инженерии можно направленно улучшить свойства микроорганизма для получения регулируемой экспрессии того или иного гена, кодирующего информацию о нужном продукте. Например, гены, несущие информацию о необходимом продукте, могут быть модифицированы in vitro для того, чтобы удалить сайты связывания, которые подавляют синтез продукта по механизму обратной связи. Затем рекомбинантную ДНК вновь встраивают в геном микроорганизма-продуцента. Подобным методом в бактериальную клетку могут быть введены и чужеродные гены, которые обеспечат работу новых метаболитических путей, в этом случае организмы называют трансгенными.
Трансгенные микроорганизмы, содержащие чужеродные гены, могут использовать дешёвые субстраты или синтезировать новые продукты, не свойственные данному организму. То есть новые штаммы можно конструировать в направлении изменения их метаболизма, и это направление в генетической инженерии называется биохимической, или метаболитической, инженерией. В то же время новые штаммы можно конструировать и в направлении их приспособления к специальным требованиям технологического процесса, и это направление называется технологической инженерией.
Генетическое конструирование новых штаммов-продуцентов требует глубоких знаний генетики используемого объекта (микроорганизма). В современных условиях определить последовательность генов, т. е. провести полное секвенирование генома нужного вида бактерий, можно в течение нескольких месяцев.
Среди грамотрицательных бактерий наиболее изученным объектом является Escherichia coli, которая служит моделью для анализа регуляции метаболитических потоков и широко используется для получения рекомбинантных белков и такого синтеза некоторых соединений (аминокислот, витаминов и др.).
Наиболее изученный объект среди грамположительных бакте- рий – Bacillus subtilis, которая является продуцентом разнообразных внеклеточных протеаз, используемых как добавки в моющие средства (рис. 17).
В настоящее время продолжается анализ генома бактерий Corynebacterium glutamicum, которые являются продуцентами аминокислот и нуклеотидов в промышленных производствах.

Рис. 17. Продуценты аминокислот и нуклеотидов: клетки Bacillus subtilis (А) и Corynebacterium glutamicum (Б)
Наибольший интерес для конструирования новых штаммов бактерий-суперпродуцентов представляют микроорганизмы, обитающие в экстремальных условиях (при высоких давлении и солености воды, температурах выше точки кипения воды и др.). Предполагают, что эти бактерии можно будет использовать в промышленности при получении высокостабильных ферментов. Например, бактерии вида Archaeoglobus fulgidus хорошо растут при высоких давлении и температуре, и их обычно обнаруживают в глубине нефтяных скважин. Ферменты, которые продуцируют эти бактерии, можно будет применять для новых технологий очистки промышленных или военных объектов или для переработки отходов различных продуктов.
§ 11.2. Возможный риск применения генетически модифицированных организмов и пути его преодоления
Технологии создания рекомбинантных ДНК являются очень важным инструментом в микробиологических исследованиях, но в отношении широкого применения генетической инженерии ещё в самом начале (середина 70-х гг. ХХ в.) её развития многие генетики выражали беспокойство по поводу возможного риска создания новых генетических структур и их бесконтрольного распространения в окружающей среде. В связи с этим многие страны приняли законы о контроле за применением технологии рекомбинантной ДНК (табл. 6). Например, в 1975 г. была проведена Азиломарская конференция по вопросам технологии рекомбинантной ДНК, принявшая рекомендацию об установлении моратория на определённые эксперименты до тех пор, пока не будет достаточно оценён их возможный риск. В частности, было принято требование предотвращать случайное или сознательно допускаемое попадание в окружающую среду организмов, подвергшихся обработке методами генетической инженерии (генетически модифицированных организмов, «ГМО»), которые в результате неконтролируемого роста могли бы стать, например, «бактериями-убийцами». Способность размножаться после попадания в окружающую среду, отличающая, ГМО от других опасных агентов (например, физических, таких как радиация, или химических, таких как яды), и возможность переноса генов от ГМО в любой другой организм и экспрессии в нём чужеродных генов (т. е. не планируемое возникновение трансгенных организмов) были и остаются двумя главными факторами риска, связанного с применением рекомбинантных ДНК.
Таблица 6 Государственные решения и законы о контроле за применением технологии рекомбинантной ДНК в США, Японии и Европе (по Й. Ленгелеру)
|
№ п/п
|
Год
|
Событие, директивы
|
|
США
|
||
|
1
|
1972
|
Первые эксперименты с рекомбинантной ДНК
|
|
2
|
1973
|
Гордонская исследовательская конференция по нуклеиновым кислотам: первое обсуждение риска, связанного с генной инженерией
|
|
3
|
1974
|
Опубликованные Полом Бергом письма с предложением о введении моратория на определённые эксперименты
|
|
4
|
1975
|
Азиломарская конференция: спонтанный мораторий на определённые эксперименты, связанные с технологией рекомбинантной ДНК
|
|
5
|
1976
|
Первые указания для исследований с применением рекомбинантной ДНК, опубликованные Национальным институтом здоровья
|
|
Япония
|
||
|
1
|
1979
|
«Указания для экспериментов с рекомбинантной ДНК», разработанные Агентством науки и технологии и Министерством образования
|
|
2
|
1986
|
«Указания для промышленного применения технологии рекомбинантной ДНК», разработанные Министерством внешней торговли и промышленности и Министерством здравоохранения
|
|
3
|
1989
|
«Указания для применения организмов с рекомбинантной ДНК в сельском, лесном и рыбном хозяйствах и других родственных сферах хозяйственной деятельности», разработанные Министерством сельского, лесного и рыбного хозяйства
|
|
4
|
1991
|
«Указания для оценки безопасности продуктов питания и пищевых добавок, создаваемых с применением метода рекомбинантной ДНК», разработанные Министерством здравоохранения
|
|
Европа
|
||
|
1
|
1978
|
«Указания для защиты от опасности, связанной с рекомбинантной ДНК in vitro», разработанные правительством Федеративной Республики Германия
|
|
2
|
1986
|
«Акт об окружающей среде и генной технологии» в Дании
|
|
3
|
1989
|
«Законодательство о работе в области генетики» в Великобритании
|
|
4
|
1990
|
Директивы Европейского сообщества, касающиеся ограничения использования генетически модифицированных организмов (90/219/ЕЕС) и произвольного высвобождения их в окружающую среду (90/220/ЕЕС)
|
|
5
|
1990
|
Принятие германского «Акта о генной инженерии»
|
|
6
|
1993
|
Первое исправление германского «Акта о генной инженерии»
|
Поэтому в целях безопасности первыми объектами в технологии рекомбинантной ДНК были генетически дефективные микробные штаммы, чаще всего ауксотрофные мутанты, которые не могут расти на питательных средах в отсутствии какого-либо вещества и редко встречаются в природной среде. Так же для этих целей используют и температурочувствительных мутантов, которые не могут расти при температуре тела человека и теплокровных животных.
Библиографический список
- Бабаева, И. П. Биология почв / И. П. Бабаева, Г. М. Зенова. – М. : Изд-во МГУ, 1989. – 336 с.
- Беляев, С. С. Метанобразующие бактерии: Биология, систематика, применение в биотехнологии / С. С. Беляев // Успехи микробиологии. – 1988. – Т. 2. – С. 169.
- Воробьёва, Л. И. Промышленная микробиология / Л. И. Воробьёва. – М. : Изд-во МГУ, 1989. – 294 с.
- Гельцер, Ю. Г. Биологическая диагностика почв / Ю. Г. Гельцер. – М. : Изд-во МГУ, 1986. – 81 с.
- Готтшалк, Г. Метаболизм бактерий / Г. Готтшалк. – М. : Мир, 1982. – 310 с.
- Гринюс, Л. Л. Транспорт макромолекул у бактерий / Л. Л. Гринюс. – М. : Наука, 1986. – 210 с.
- Громов, Б. В. Экология бактерий / Б. В. Громов, Г. В. Павленко. – Л. : Изд-во ЛГУ, 1989. – 248 с.
- Дуда, В. И. Архебактерии в системе царств органического мира / В. И. Дуда, А. В. Лебединский, В. В. Кривенко // Успехи микробиологии. – 1985. – Т. 20. – С. 3.
- Емцев, В. Г. Микробиология / В. Г. Емцев, Е. Н. Мишустин. – М. : Дрофа, 2005. – 446 с.
- Жизнь микробов в экстремальных условиях / под ред. Д. Кашнера. – М. : Мир, 1981. – 519 с.
- Завальский, Л. Ю. Хемотаксис бактерий / Л. Ю. Завальский, А. В. Лазарев, В. Г. Попов // Успехи микробиологии. – 1989. – Т. 23. – С. 3.
- Звягинцев, Д. Г. Почва и микроорганизмы / Д. Г. Звягинцев. – М. : Изд-во МГУ, 1987. – 226 с.
- Иерархическая система биоиндикации почв, загрязненных тяжелыми металлами / Е. И. Андреюк [и др.] // Почвоведение. – 1977. – № 12. – С. 1492 – 1496.
- Кондратьева, Е. Н. Хемолитотрофы и метилотрофы / Е. Н. Кондратьева. – М. : Изд-во МГУ, 1983. – 176 с.
- Кондратьева, Е. Н. Фототрофные микроорганизмы / Е. Н. Кондратьева, И. В. Максимова, В. Д. Самуилов. – М. : Изд-во МГУ, 1989. – 375 с.
- Лурия, С. Общая вирусология / С. Лурия, Дж. Дарнелл, Д. Балтимор [и др.]. – М. : Мир, 1981. – 680 с.
- Льюин, Б. Гены / Б. Льюин. – М. : Мир, 1987. – 544 с.
- Маргелис, Л. Роль симбиоза в эволюции клетки / Л. Маргелис. – М. : Мир, 1983. – С. 165. – 181.
- Методы почвенной микробиологии и биохимии / под ред. Д. Г. Звягинцева. – М. : Изд-во МГУ, 1991. – 304 с.
- Промышленная микробиология / под ред. Н. С. Егорова – М. : Высш. шк., 1989. – 687 с.
- Современная микробиология. Прокариоты : в 2 т. / под ред. Й. Ленгера, Г. Древса, Г. Шлегеля. – М. : Мир, 2005. – Т.1. – 654 с.; Т. 2. – 493 с.
- Стейниер, Р. Мир микробов : в 3 т. / Р. Стейниер, Э. Эдельберг, Дж. Ингрэм. – М. : Мир, 1979. – Т. 1 – 320 с.; Т. 2 – 334 с.; Т. 3. – 486 с.
- Стент, Г. Молекулярная генетика / Г. Стент. – М. : Мир, 1974. – 536 с.
- Троценко, Ю. А. Энергетический метаболизм метилотрофных бактерий / Ю. А. Троценко, Е. В. Четина // Успехи микробиологии. – 1988. – Т. 22. – С. 3.
- Хмель, И. А. Плазмиды и эволюция микроорганизмов / И. А. Хмель // Успехи современной биологии. – 1985. – Т. 99. – 323 с.
- Шлегель, Г. Общая микробиология / Г. Шлегель. – М. : Мир, 1987. – 478 с.
- Bergey's Manua1 of Systematic Bacteriology. – Ba1timore; Hong Kong; London; Sydney. – 1984, 1986, 1989. – Vо1. 1 – 4.
- The Biology of anaerobic microorganisms / Ed. А. J. В. Zennder. – .Y. е. а., 1988.
- The Prokaryotes. А handbook оn habitats, iso1ation and identification of bacteria. – Ber1in; Heide1berg; NewYork; SpringerVer1ag, 1981. – Vо1. 1,2.
- Virus Taxonomy. Classification and Nomenclature of Viruses / Ed. M.D.Summers. – Springfr-Verlag; Wien; New York, 1999.
Дополнительный материал:

